Rutiner for helseforskning
Rutinene gjelder for medisinske og helsefaglige forskningsprosjekter. Dette omfatter forskning på mennesker, humant biologisk materiale og helseopplysninger. Pilotstudier og utprøvende behandling er også inkludert i rutinene.
Rutinene for helseforskning er basert på kravene i helseforskningsloven og tilhørende forskrifter og retningslinjer. De skal være et praktisk hjelpemiddel for forskere i alle faser av et forskningsprosjekt. Det er viktig å merke seg at rutinene kun gjelder for forskningsprosjekter som omfattes av helseforskningslovens virkeområde. For mer informasjon om forskningsetikk og retningslinjer, vises det til UiTs nettside om forskning og innovasjon.
Spørsmål om kvalitetssystemet for helseforskning?
Seksjon for forskning, utdanning og formidling ved Det helsevitenskapelige fakultet (FUF HF) forvalter dette kvalitetssystemet. Kvalitetssystemet blir gjennomgått og endret etter behov. Har du spørsmål eller forslag til forbedring, send oss gjerne en e-post: helseforskning@helsefak.uit.no
Rutiner for planlegging og oppstart av et forskningsprosjekt
Forskningsprosjektet skal alltid være forankret ved en forskningsansvarlig institusjon. Forankringen på UiT skjer ved skriftlig bekreftelse fra instituttleder om at prosjektet kan igangsettes. Prosjektleder må kunne fremvise denne bekreftelsen ved forespørsel.
Særlig om forankring av prosjekter når ansatte har stilling både på UiT og UNN
Prosjektlederen har ansvaret for å sikre forankringen, enten ved UiT eller UNN. Samarbeidsavtalen mellom UiT og UNN regulerer hvem som skal være forskningsansvarlig institusjon der prosjektleder har stilling ved begge institusjoner. Avtalen finnes her: Avtale om organisering og forankring av forskningsprosjekter mellom UNN og UiT
For samarbeidsprosjekter mellom UiT og UNN gjelder overnevnte avtale.
Endring av arbeidssted
Dersom prosjektleder slutter ved UiT eller endrer institutt tilhørighet i løpet av prosjektperioden eller etter at prosjektet er avsluttet, må ansvaret for å ivareta prosjektet og forskningsdata avklares med instituttleder. REK og Sikt skal også varsles om slik endring. Dersom ansvaret ikke overdras til en ansatt i stilling på samme nivå eller ikke lar seg avklare, flyttes ansvaret oppover til instituttleder eller dekan. Eierskap og ansvar for prosjektet og forskningsdata kan også overføres til en annen institusjon. Dette må i så tilfelle avtalefestes, og dataene bør ha en merking som viser hvilken institusjon de er overført fra og hvor forskningen er utført.
Multisenterstudie
Med multisenterstudier forstås forskningsprosjekter som finner sted ved flere virksomheter samtidig og etter samme protokoll.
En multisenterstudie skal ha én prosjektleder. Prosjektleder skal koordinere aktivitetene og sørge for å innhente forhåndsgodkjenning fra REK og sikre at den forskningsansvarlige ved de øvrige deltagende virksomheter er informert om forskningsprosjektet før prosjektet startes.
I internasjonale multisenterstudier skal det være en angitt norsk prosjektleder for de deler som finner sted i Norge, og denne informerer de deltagende norske virksomheter tilsvarende.
Sist endret: 12.02.2026
Printvennlig innhold: Forankring av forskningsprosjektet
Prosjektleder må avklare behov for nødvendige avtaler med samarbeidende forskere og forskningsinstitusjoner, for eksempel samarbeidsavtale, Material Transfer Agreement (MTA) eller utleveringsavtale.
Ved usikkerhet om hvilke avtaler som kreves, kan FUF HF kontaktes for veiledning.
Avtalemaler finnes tilgjengelig på UiTs intranett.
Sist endret: 12.02.2026
Printvennlig innhold: Avklar behov for nødvendige avtaler
Før et forskningsprosjekt settes i gang, må det avklares om prosjektet er helseforskning, kvalitetssikring eller annen forskning.
Denne avklaringen er avgjørende for hvilke lover, regler og godkjenninger som gjelder. Det er formålet med prosjektet som bestemmer kategorien.
Medisinsk og helsefaglig forskning: Helseforskning har som formål å skaffe ny kunnskap om helse og sykdom. Slike prosjekter reguleres av helseforskningsloven med tilhørende forskrift, og må ha forhåndsgodkjenning fra REK (Regionale komiteer for medisinsk og helsefaglig forskningsetikk). Bruk av vitenskapelig metode, innsamling av helseopplysninger eller planer om publisering er ikke alene nok til at prosjektet regnes som helseforskning – det avgjørende er formålet om ny kunnskap om helse og sykdom.
Annen forskning: Prosjekter som undersøker forhold knyttet til helse eller sykdom, men uten formål om ny kunnskap om helse og sykdom, regnes som annen forskning. Disse faller utenfor helseforskningslovens virkeområde.
Kvalitetssikring: Kvalitetssikring har som formål å vurdere om diagnostikk og behandling fungerer som forventet, altså om praksis holder ønsket kvalitet.
Slike prosjekter er en del av helsetjenestens ordinære virksomhet og krever ikke REK-godkjenning. De reguleres av de lover og regler som gjelder for helsetjenesten.
Dersom det er tvil om et prosjekt er fremleggingspliktig til REK, kan prosjektleder sende inn en fremleggingsvurdering. REK vil da vurdere om prosjektet krever forhåndsgodkjenning, uten at det er nødvendig å utarbeide en full søknad.
Sist endret: 21.11.2025
Printvennlig innhold: Avklar formålet med prosjektet
Forskningsprotokoll
For hvert forskningsprosjekt skal det utarbeides en forskningsprotokoll som skal angi minst:
- prosjektleder
- en vitenskapelig utformet prosjektplan med angivelse av prosjektets formål, begrunnelse, materiale, metoder, sannsynliggjøring av at valgt studiedesign kan gi svar på forskningsspørsmålet og anslåtte tidsrammer for prosjektet
- hvordan helseopplysninger skal behandles, herunder fra hvilke kilder helseopplysninger skal innhentes og om slike opplysninger skal utleveres til andre eller overføres til land utenfor EØS
- fra hvilke kilder humant biologisk materiale skal uttas og om slikt materiale skal utleveres til andre eller overføres til utlandet
- vurdering av forskningsetiske utfordringer ved prosjektet, særlig nytte-risiko aspektet for forskningsdeltakere finansieringskilder, interesser og avhengighetsforhold, herunder forskere og forskningsdeltakeres eventuelle økonomiske forhold knyttet til det aktuelle forskningsprosjektet
- plan for offentliggjøring av resultater og opplysninger om mulig utvidet bruk, herunder kommersiell bruk, av forskningsresultater, data eller biologisk materiale
REK kan kreve nærmere opplysninger i forskningsprotokollen før endelig vedtak blir fattet.
Datahåndteringsplan
I henhold til prinsipper og retningslinjer for forvaltning av forskningsdata ved UiT stilles det krav til alle forskningsprosjekt ved UiT skal ha en plan for hvordan data samles inn, bearbeides, arkivers og deles åpent – datahåndteringsplan (DHP). Mer informasjon om DHP og maler finner tilgjengelig i forskningsportalen.
Risikovurdering
I henhold til ledelsessystem for sikkerhet, beredskap og personvern ved UiT skal alle forskningsprosjekter som behandler helse- og personopplysninger risikovurderes i henhold informasjonssikkerhet og personvern, og evt. HMS dersom det er behov.
Ytterligere informasjon og skjema finnes her:
Brukermedvirkning i helseforskningSist endret: 13.03.2026
Printvennlig innhold: Krav til forskningsprotokoll, datahåndteringsplan og risikovurdering
Før igangsettelse skal instituttleder ha godkjent forskningsprosjektet. Forskningsprosjekt som faller inn under medisinsk og helsefaglig forskning krever godkjenning fra REK. Ved behandling av personopplysninger skal prosjektet meldes inn til Sikts personverntjeneste for forskning.
REK skal forhåndsgodkjenne alle helseforskningsprosjekter som involverer mennesker, humant biologisk materiale eller helseopplysninger. Prosjektleder skal sørge for at søknad, inkludert forskningsprotokoll og annen dokumentasjon sendes til REK for behandling. Mer informasjon om REK og søknad om godkjenning er finner her: REK portalen
Sikts personverntjenester bistår UiT med å sikre og påvise at behandling av personopplysninger til forskningsformål skjer i samsvar med personvernregelverket. Prosjektleder skal melde fra til Sikt gjennom dette meldeskjemaet. Meldeskjemaet bør være mest mulig fullstendig for å unngå forsinkelser av prosjekter, da vurdering fra Sikt må foreligge før prosjekter kan igangsettes.
Personvernkonsekvensvurdering (DPIA)
I de tilfeller behandling av personopplysning fører til høy risiko for fysiske personer rettigheter og friheter skal det gjennomføres en DPIA. Mer informasjon om dette finnes her: personvernkonsekvensvurdering
Gjennomføre et prosjekt anonymt
Prosjekter der det kun skal benyttes anonyme opplysninger, behøver ikke å meldes til Sikt eller forhåndsgodkjennes av REK. Det kreves heller ikke samtykke ved bruk av anonyme data. Merk at det er forskjell på å gjennomføre et prosjekt anonymt og å anonymisere opplysningene. En behandling blir regnet som anonym dersom det ikke er mulig å identifisere enkeltpersoner på noe tidspunkt av datainnsamlingen. Det skal da heller ikke eksistere en koblingsnøkkel. For innhenting av materiale og opplysninger som senere skal anonymiseres kreves det samtykke, og prosjektet skal forhåndsgodkjennes av REK og meldes til Sikt på vanlig måte.
Andre aktuelle godkjenningsinstanser
| Type forskningsprosjekt | Godkjenningsinstans |
| Klinisk utprøving av legemidler på mennesker | Komiteene for klinisk utprøving av legemidler og medisinsk utstyr (REK KULMU) og Direktoratet for medisinske produkter (DMP) via Clinical Trial Information System (CTIS) |
| Klinisk utprøving av medisinsk utstyr | Komiteene for klinisk utprøving av legemidler og medisinsk utstyr (REK KULMU) og Direktoratet for medisinske produkter (DMP) |
| Forskning der kosttilskudd, naturmidler eller andre stoffer inntas | Regional etisk komité (REK) og Direktoratet for medisinske produkter (DMP) |
| Forskning som omfatter anvendelse av stråling på mennesker | Regional etisk komité (REK) og Direktoratet for strålevern og atomsikkerhet (DSA) |
| Helseforskning som involverer medisinsk bruk av bioteknologi m.m. og hvor det forventes funn av helsemessig betydning for deltakeren eller hvor opplysninger planlegges ført tilbake til deltakeren. | Regional etisk komité (REK) og Helsedirektoratet (Bioteknologinemda) |
| Registerstudier | For forskning på helseopplysninger (registerstudier), må det søkes dataansvarlig om tilgang til dataene og om nødvendig dispensasjon fra taushetsplikten |
Sist endret: 21.11.2025
Printvennlig innhold: Godkjenning og innmelding
Rutiner for gjennomføring av et forskningsprosjekt
I forskningsprosjekter som skal behandle helse- og personopplysninger må prosjektleder sørge for å ha et rettslig behandlingsgrunnlag før opplysningene hentes inn. De mest aktuelle behandlingsgrunnlagene for forskning er samtykke og allmennhetens interesse. Samtykke som behandlingsgrunnlag må ikke forveksles med forskningsetisk samtykke, eller samtykke etter helseforskningsloven. Krav om samtykke til å delta i forskning gjelder uavhengig av hvilke behandlingsgrunnlag som er benyttet.
Innen helseforskning er den klare hovedregelen at deltakelse skal være basert på et informert, frivillig, uttrykkelig og dokumenterbart samtykke. Unntak fra denne hovedregelen skal begrunnes og må godkjennes av REK.
Behandlingsgrunnlag
Prosjektleder er ansvarlig for at behandlingen av helse- og personopplysninger i prosjektet oppfyller kravene i personvernforordningen (GDPR) og øvrige bestemmelser.
All behandling av personopplysninger må ha et rettslig grunnlag i personvernforordningen artikkel 6. I forskningsprosjekter kan både samtykke (artikkel 6 nr. 1 bokstav a) og allmennhetens interesse (artikkel 6 nr. 1 bokstav e) være aktuelle rettslige grunnlag. For behandling av særlige kategorier personopplysninger, slik som helseopplysninger, kreves det i tillegg at et av vilkårene i artikkel 9 nr. 2 er oppfylt.
Noen behandlingsgrunnlag krever også et supplerende rettslig grunnlag, som regel etter personopplysningsloven §§ 8 og 9. Avhengig av hvilke kilder helse- og personopplysninger innhentes fra, kan det være ulike lover og regler innen helselovgivningen man må forholde seg til, som for eksempel helsepersonelloven, helseregisterloven og forskrift om medisinske kvalitetsregistre.
Informasjonsplikt
I alle forskningsprosjekter der det samles inn personopplysninger er det pålagt å informere forskningsdeltakere om behandlingen av personopplysningene deres.
Informasjonen skal være kortfattet og lett forståelig. Det anbefales å bruke klart og enkelt språk tilpasset målgruppen. Informasjonen skal som hovedregel være skriftlig, da det skal være mulig å dokumentere hvilken informasjon som har blitt gitt. Les mer om hva som skal til for å oppfylle kravene til informasjon på Sikt sine nettsider: Informasjon til deltakere i forskningsprosjekt
I noen tilfeller kan det gjøres unntak fra informasjonsplikten, for eksempel der dataene er anonyme, der det er umulig eller uforholdsmessig vanskelig å informere eller der forskningsdeltakeren er kjent med egen deltakelse i prosjektet. Unntak fra informasjonsplikten skal være godt begrunnet i meldeskjemaet for personopplysninger til Sikt.
For forskningsprosjekter som faller inn under virkeområdet til helseforskningsloven anbefales det at informasjonsskriv og samtykke utarbeides i henhold til mal fra REK.
Samtykke
Helseforskningsloven stiller klare krav til hva som kvalifiserer til et gyldig samtykke. Loven sier også noe om hvem som kan avgi samtykke, og hvor lenge det kan oppbevares. Det er viktig å passe på at alle samtykkeskjemaene er datert og signert på en slik måte at det er mulig å identifisere deltakeren fra signaturen. Dette kan løses ved at deltakerens navn skrives i blokkbokstaver i tillegg til signaturen.
For at et samtykke skal være gyldig, må det være:
- frivillig
- spesifikt
- informert
- utvetydig
- gitt gjennom en aktiv handling
- dokumenterbart
- mulig å trekke tilbake like lett som det ble gitt
Samtykket skal i utgangspunktet bygge på spesifikk informasjon om et konkret forskningsprosjekt. For forskningsformål er det åpent for at forskningsdeltakere kan samtykke til at humant biologisk materiale og helseopplysninger kan brukes til nærmere bestemte, bredt definerte forskningsformål. Deltakere som har avgitt bredt samtykke har krav på jevnlig informasjon om prosjektet.
Dersom forskningsdeltakeren kan anses å være i et slikt avhengighetsforhold til den som ber om samtykke at forskningsdeltakeren vil kunne føle seg presset til å gi samtykke, skal samtykket innhentes av en annen som forskningsdeltakeren ikke har slikt forhold til.
Samtykkeskjema må signeres og dateres. Det skal fremkomme tydelig hvem som har signert samtykkeskjema, det anbefales derfor å skrive navn i blokkbokstaver i tillegg til signatur. For digitale samtykkeskjema hvor det trykkes på en knapp eller hakes av i en boks på en nettside eller i en app, kan man ta vare på teknisk informasjon fra økten for å oppfylle kravet til dokumentasjon.
Ved endring i prosjektet eller endringer i bruk av data (eksempelvis at data skal sendes ut av EU) må det vurderes om det er nødvendig å innhente nytt samtykke. Nytt samtykke skal sendes til REK sammen med endringssøknad, og må være godkjent av REK før det tas i bruk.
Unntak fra samtykke kan bare skje dersom REK vurderer det slik at forskningen er av vesentlig interesse for samfunnet, og at hensynet til deltakernes velferd og integritet er ivaretatt. Det er prosjektleders ansvar å begrunne eventuell søknad om unntak fra samtykke.
Innhenting av samtykke fra barn, unge og personer uten samtykkekompetanse
Det er egne regler for innhenting av samtykke fra barn eller andre uten samtykkekompetanse:
- For barn og unge under 16 år må begge foreldre, eller andre med foreldreansvar, samtykke til barnets deltagelse
- Barn og unge mellom 12 og 16 år har i visse forskningsprosjekter selv rett til å samtykke til deltakelse i helseforskningsprosjekter, jf. Forskrift om barn mellom 12 og 16 år sin rett til selv å samtykke til deltakelse i medisinsk og helsefaglig forskning
- Ungdom over 16 år skal samtykke på egen hånd
- Ved forskning som innebærer legemsinngrep eller legemiddelutprøvinger, skal ungdom mellom 16 og 18 år samtykke sammen med foresatte
- For personer uten samtykkekompetanse (pga. helsetilstand, psykisk utviklingshemming eller umyndiggjøring) skal nærmeste pårørende samtykke. Merk at helseforskningsloven § 18 har visse tilleggsvilkår som må være oppfylt for forskning som inkluderer disse gruppene
Kollektivt samtykke i samisk helseforskning
Samisk helseforskning omfatter alle forskningsprosjekter hvor samer som gruppe inngår, eller som innhenter data fra områder hvor samer utgjør en betydelig andel av befolkningen, eller som omhandler samisk språk, kultur eller historie.
Før et samisk helseforskningsprosjekt kan settes i gang, skal det foreligge et kollektivt samtykke i henhold til gjeldende etiske retningslinjene for samisk helseforskning. Kollektivt samtykke vil si at en sakkyndig etisk komité for samisk helseforskning, utpekt av Sametinget, skal godkjenne prosjektene. Godkjenningen kommer i tillegg til forhåndsgodkjenning fra REK, rettslig behandlingsgrunnlag og individuelt samtykke.
Dersom du er usikker på om ditt prosjekt trenger et samisk kollektivt samtykke, kan du sende inn en fremleggingsvurdering til sakkyndig etisk komité for samisk helseforskning.
Oppbevaring av samtykke
Det må kunne dokumenteres at gyldig samtykke er innhentet så lenge personopplysninger behandles. Signerte samtykkeerklæringer i papirformat skal oppbevares forsvarlig i låst skap. Digitale samtykkeerklæringer skal oppbevares forsvarlig på et område uten tilgang for uvedkommende. Digitale samtykkeerklæringer må lagres på en slik måte at det ikke er mulig å redigere erklæringene.
Av dokumentasjonshensyn skal prosjektdata inkludert samtykkeskjema oppbevares i fem år etter at prosjektet er avsluttet, dersom prosjektet har hatt godkjenning fra REK. Etter dette tidspunktet skal samtykkeerklæringene slettes/makuleres. For prosjekter som ikke er framleggingspliktig, skal samtykkeskjema slettes ved prosjektets slutt.
Tilbaketrekking av samtykke
Et samtykke skal når som helst kunne trekkes tilbake uten negative konsekvenser for deltaker. Deltaker skal informeres om retten til å trekke samtykke i informasjonsskriv eller tilsvarende. Ved tilbaketrekking av samtykke må forskningen på deltakerens biologiske materiale eller helseopplysninger opphøre.
Den som trekker tilbake samtykket, kan kreve at det biologiske materialet destrueres og at helseopplysningene slettes eller utleveres innen 30 dager. Dette gjelder ikke dersom materialet eller opplysningene er anonymisert, dersom de inngår i et annet biologisk produkt eller opplysningene allerede er inngått i utførte analyser. REK kan bestemme at sletting eller utlevering av materialet skal utsettes til forskningsprosjektet er gjennomført.
Informasjonsplikt ved skade og forsikring
Dersom forskningen innebærer økt risiko for deltakerne, skal prosjektleder sørge for at dette er informert om på forhånd. I tilfelle skade eller komplikasjoner som følge av prosjektet, må prosjektleder informere deltakeren og gjøre dem kjent med rettighetene til erstatning, for eksempel gjennom Norsk Pasientskadeerstatning eller andre forsikringsordninger. Staten er selvassurandør. Det innebærer at staten som hovedregel ikke tegner forsikring, men håndterer tap og skader når de oppstår.
Reservasjonsrett
Deltakere har rett til å reservere seg mot at deres biologiske materiale blir brukt i forskning. Prosjektleder har et ansvar for at deltakerne blir informert om muligheten til å registrere seg i et reservasjonsregister, og at forskningsdeltakernes ønsker blir håndtert med respekt.
Taushetsplikt og innsyn
Alle som håndterer person- og helseopplysninger i et forskningsprosjekt, er underlagt taushetsplikt. Prosjektleder må sørge for at deltakerne er klar over at de kan få innsyn i hvilke helseopplysninger som er samlet inn om dem, og at de kan kreve at uriktige opplysninger kan slettes.
Sist endret: 12.02.2026
Printvennlig innhold: Behandlingsgrunnlag, informasjonsplikt og samtykke
Forskningsdata har stor verdi og det er viktig at de lagres forsvarlig for å sikre at data ikke går tapt eller blir reduserte i kvalitet. Behandling og oppbevaring av forskningsdata kan være utfordrende, spesielt med store datasett eller data som setter spesielle krav til sikkerhet. Mer informasjon om forvaltning av forskningsdata er tilgjengelig i Forskningsdataportalen.
Prosjektleder må sørge for at:
- det foreligger en datahåndteringsplan
- forskningsdata lagres og behandles fortløpende på en sikker måte i henhold til Ledelsessystem for sikkerhet, beredskap og personvern og prinsipper og retningslinjer for forvaltning av forskningsdata ved UiT.
- forskningsdata behandles i de løsninger UiT har godkjent, basert på risikovurdering og klassifisering av informasjonsverdier. Dersom det benyttes utstyr som ikke tilhører UiT skal kravene i rutine for bruk av privat utstyr ved behandling av personopplysninger i forsknings- og studentprosjekter følges
- papirbasert forskningsdata som ikke er anonymisert oppbevares i låst skap eller lignende. Det samme gjelder samtykkeskjema, intervjuskjema, observasjonsnotater eller andre papirbaserte notater. Dette gjelder også lyd-, bilde- og videoopptak
- forskningsdata kun er tilgjengelig for de medarbeiderne som skal delta i forskningsprosjektet, og at det føres en oversikt over hvem som har tilgang. I tilfeller der det er eksterne prosjektmedarbeidere skal avtale signeres før det gis tilgang
- forskningsdataen kun behandles i det tidsrom som er angitt i forskningsprotokollen og så lenge gyldig godkjenning fra REK evt. også andre instanser foreligger. Bruk av data utover denne perioden krever godkjenning av REK og evt. også andre instanser. Personverntjenesten hos Sikt skal også varsles dersom forskningsdata skal behandles utover opprinnelig tiltenkt periode
- forskningsdata oppbevares pseudonymt (avidentifisert). Dette innebærer at identifiserbare opplysninger erstattes med koder, men at det fortsatt finnes en koblingsnøkkel som gjør det mulig å koble dataene tilbake til forskningsdeltaker. Koblingsnøkkel og forskningsdata skal alltid lagres hver for seg
Oversikt over tilgjengelige løsninger for oppbevaring av forskningsdata ved UiT er tilgjengelig her: lagringsløsninger
Sist endret: 12.02.2026
Printvennlig innhold: Behandling og lagring av aktiv forskningsdata
Prosjektet skal utføres i henhold til forskningsprotokollen og i samsvar med det som er angitt i melding til Sikt og i godkjenning fra REK – samt evt. andre instanser. Likevel kan det oppstå endringer underveis som kan føre til plikt til å varsle om endringer.
Eksempler på endringer som kan medføre meldeplikt er:
- endring av forskningsansvarlig institusjon, ved eksempelvis bytte fra UiT til UNN
- endring av prosjektleder eller prosjektmedarbeidere
- endringer i utvalg, for eksempel økning i antall deltakere eller inkludering av nye grupper
- endringer i design og analyse
- endringer i varighet, ved for eksempel utsettelse eller forlengelse av prosjektperioden
- endring i typer persondata som skal samles inn
Dersom endringen av forskningsprosjektet er så stor at det må anses å være et helt nytt prosjekt, må prosjektleder melde det som et nytt prosjekt. Ved endringer i organisering, eksempelvis ved endring av prosjektleder eller forskningsansvarlig institusjon skal instituttleder og FUF HF varsles.
Melding om endring til Sikt gjøres via Min forskning og endringer til REK sendes via REK-portalen
Endring må meldes og godkjennes før endringene blir iverksatt. Merk at søknad om forlengelse av prosjektperiode må sendes til REK i god tid før opprinnelige periode godkjent av REK utløper.
Sist endret: 12.02.2026
Printvennlig innhold: Endring av forskningsprosjektet
Rutiner for avslutning av et forskningsprosjekt
Behandling av helse- og personopplysninger i helseforskning er av midlertidig art. Ved prosjektavslutning skal opplysninger, dokumenter og humant biologisk materiale forsvarlig langtidsoppbevares, anonymiseres eller slettes/destrueres i tråd med vedtak fra REK.
Prosjektleder skal ved prosjektslutt:
- vurdere om materialet skal anonymiseres, slettes eller langtidsoppbevares
- sende sluttmelding til REK senest 6 måneder etter at godkjenningsperioden er utløpt
- melde prosjektet avsluttet hos Personverntjenesten hos Sikt
- sende sluttrapport til eventuelle finansieringskilder
- sende sluttmelding til evt. andre registre
Plikt til lagring
I noen sammenhenger kan det være oppbevaringsplikt for forskningsdataene av hensyn til etterkontroll og tilsyn.
- REK kan av kontrollhensyn kreve at forskningsdata skal oppbevares i inntil fem år etter prosjektslutt
- Forskningsprosjekter som er finansiert av midler fra EU og Norges forskningsråd kan kreve at data lagres i henholdsvis 5 og 10 år
- Andre kontraktsbestemmelser kan også tilsi lengre lagringstid
- Enkelte helseopplysninger kan være oppbevaringspliktige etter journalforskriften eller arkivloven
- Noen vitenskapelige tidsskrifter krever at forskningsdata oppbevares og gjøres tilgjengelig i et visst antall år etter publisering. Slike krav gir imidlertid ikke rett til å oppbevare data utover det som er godkjent av REK
Sist endret: 11.02.2026
Printvennlig innhold: Avslutning av forskningsprosjektet
Som hovedregel skal forskningsdata anonymiseres eller slettes når prosjektet er avsluttet, med mindre forskningsdata skal oppbevares for etterkontroll eller fremtidige forskningsformål. Anonymisering innebærer at alle direkte og indirekte identifiserende opplysninger fjernes permanent, og at det ikke lenger er mulig å koble dataene til enkeltpersoner. Dette betyr at koblingsnøkkelen må slettes, og at anonymiseringen må være reelt irreversibel. Dersom kun koblingsnøkkelen slettes, vil forskningsfilen ikke anses som slettet. I noen tilfeller kan det være mulig å identifisere forskningsdeltakere selv etter at koblingsnøkkelen er slettet, for eksempel hvis datamaterialet inneholder indirekte identifiserbare opplysninger. Dette kan skje når datamaterialet er lite, eller når stedstilhørighet er registrert for en sjelden sykdom. I slike tilfeller må det iverksettes ytterligere tiltak for å sikre at datamaterialet blir reelt anonymt.
Dersom det ikke er mulig å anonymisere materialet, skal forskningsdataene slettes i sin helhet. Dette omfatter forskningsfiler, e-poster, notater, samtykkeskjemaer, sikkerhetskopier og koblingsnøkler etc. Prosjektleder skal påse at eventuelle kopier av data hos prosjektmedarbeidere fjernes.
I arbeidet med personopplysninger i forskning, er det avgjørende å skille mellom anonymisering og pseudonymisering (avidentifisering). Disse begrepene brukes ofte om hverandre, men har viktige forskjeller – både i praksis og i juridisk forstand. Å forveksle dem kan i verste fall føre til brudd på personopplysningsloven og helseforskningsloven.
Ved anonymisering fjernes alle identifikasjonsmuligheter fullstendig og permanent. Det finnes ingen koblingsnøkkel som kan gjøre det mulig å identifisere enkeltpersoner igjen. Dette betyr at dataene ikke lenger regnes som personopplysninger, og faller dermed utenfor personvernlovgivningen. Anonymiserte data kan brukes fritt, men det er viktig å merke seg at prosessen må være irreversibel for at dataene faktisk skal være anonymisert.
Se gjerne Datatilsynets veileder om anonymisering av personopplysninger.
Dersom prosjektleder er usikker på om forskningsdataen er tilstrekkelig anonymisert kan personvernombud ved UiT kontaktes for råd og veiledning.
Pseudonymisering innebærer at identifiserbare opplysninger erstattes med koder, men at det fortsatt finnes en koblingsnøkkel som gjør det mulig å koble dataene tilbake til individet. Dataene er dermed fortsatt å regne som personopplysninger. Pseudonymisering brukes ofte som et sikkerhetstiltak i forskning, særlig når man trenger å koble data over tid eller supplere dem med nye opplysninger. Pseudonym data er å anse som personopplysninger, fordi det i praksis kan være mulig å finne ut hvem personen er.
Reell anonymisering av data likestilles med sletting, slik at en anonymisert versjon av datasettet kan beholdes. Anonymisering innebærer at alle opplysninger, inkludert sikkerhetskopier, som kan føre til identifisering av forskningsdeltakere, slettes. Dette gjøres som regel ved at prosjektleder sletter koblingsnøkkelen.
Dersom det ikke er mulig å anonymisere materialet, må opplysningene slettes.
Sist endret: 12.03.2026
Printvennlig innhold: Sletting, anonymisering og psedunymisering av forskningsdata
Ved langtidsoppbevaring av data skal tilgangen være sterkt begrenset, og verken prosjektleder eller prosjektmedarbeidere skal ha tilgang til forskningsdataen. Ved UiT kan prosjektledere benytte seg av CLARC for langstidsoppbevaring. For mer informasjon og tilgang til tjenesten klikk deg inn på TopDesk CLARC. Tjenesten er godkjent for lagring av grønne, gule og røde data.
Inneholder forskningsdataen sensitiv informasjon (svart data) må det tas ekstra hensyn til valg av lagringsløsning. F.eks. kan Tjenester for sensitive data (TSD) benyttes. TSD er en tjeneste for lagring og analysering av strengt fortrolige data.
Kostnad til langtidsoppbevaring i for eksempel CLARC og TSD må dekkes av instituttet der forskningsprosjektet er tilknyttet. Kostnaden bør derfor være budsjettert i forskningsprosjektet, og avklart med instituttleder.
Arkivering
I tråd med prinsippene og retningslinjene for forvaltning av forskningsdata ved UiT og føringer fra Kunnskapsdepartementet, EU og Norges forskningsråd, skal data være så åpnet som mulig, og så lukket som nødvendig. Dette innebærer krav om arkivering, der forskningsdata deponeres i et egnet arkiv med mål om at andre skal kunne gjenbruke dem. Et slikt arkiv kan være enten åpent eller lukket. Dette må ikke forveksles med langtidsoppbevaring, hvor data lagres utilgjengelig og uten formål om gjenbruk.
Mer informasjon om arkivtjenester er tilgjengelig her: Forskningsdataportalen
Sist endret: 12.02.2026
Printvennlig innhold: Langstidsoppbevaring og arkivering av forskningsdata
Prosjektleder har i oppgave å sende melding til REK, Sikt og evt. andre aktuelle register ved prosjektslutt.
Sluttmelding til REK skal sendes når:
- prosjektet ikke lenger har gyldig godkjenning
- prosjektet er ferdig før utløp av godkjenning, eller
- prosjektet har fått godkjenning, men ikke igangsettes
Sluttmelding til REK skal sendes senest 6 måneder etter at godkjenningsperioden er utløpt.
Sluttmelding til REK skal bidra til å sikre både åpenhet og god kontroll. Prosjektets resultater skal presenteres objektivt og etterrettelig, og både positive og negative funn skal fremgå av meldingen.
Hvis det foreligger godkjenning fra Sikt, skal prosjektet avsluttes i Sikt.
Prosjektleder må videre sende slettemelding til aktuelle register som du har hentet data fra (eks. Norsk pasientregister, kommunalt pasient- og brukerregister).
Sist endret: 13.02.2026
Printvennlig innhold: Sluttmeldinger
Bruk av humant biologisk material (forskningsbiobank)
Video laget av Ánte Siri
Forskningsbiobanker (biobank) inneholder biologisk materiale som er samlet inn enten direkte til forskningsformål eller opprinnelig til kliniske formål og deretter tatt i bruk i forskning. Alle typer fysisk materiale som kommer fra et menneske regnes som humant biologisk materiale. Dette kan for eksempel være blod-, urin-, avførings- og spyttprøver, celle- eller vevsprøver fra ulike organer, eller hele organer.
Det skilles mellom to typer forskningsbiobanker:
- En spesifikk biobank er koblet til et konkret forskningsprosjekt.
- En generell biobank samler inn biologisk materiale til et bredt, tematisk avgrenset formål. Den generelle biobanken er ikke knyttet til et konkret forskningsprosjekt, men materialet i biobanken kan brukes til flere forskningsprosjekter innenfor biobankens formål.
Sist endret: 17.11.2025
Printvennlig innhold: Forskningsbiobank
- Utpek ansvarshavende person: Biobanken skal ha en ansvarshavende person med medisinsk eller biologisk utdanning på høyere nivå. Ansvarshavende for forskningsbiobank skal utpekes av instituttleder. Den ansvarshavende skal sørge for at biobanken opprettes og forvaltes i tråd med regelverket. Dette inkluderer å sikre at alle prosedyrer for innsamling, oppbevaring, bruk og eventuell destruksjon av materiale følges.
- Utform et dekkende samtykkeskriv: Et godt samtykkeskriv er avgjørende for bruk av biobankmateriale. Et klart og tydelig samtykke kan forhindre behovet for å innhente nytt samtykke ved ny, endret eller utvidet bruk av materialet, eller ved kobling til andre dataregistre. Generelle biobanker opprettes som regel med grunnlag i bredt samtykke.
- Forskningsprotokoll: Beskriv biobanken i prosjektets forskningsprotokoll.
- Risikovurdering:Før opprettelse, eller dersom det gjøres endringer i biobank, skal det gjennomføres en risikovurdering, som inkluderer HMS og personvern- og informasjonssikkerhet. Trykk her for mer informasjon om risikovurdering.
- Søk godkjenning fra REK: Opprettelse av en forskningsbiobank for medisinsk og helsefaglig forskning, både spesifikkog generell, krever godkjenning fra REK. Tilsvarende gjelder for ny, endret eller utvidet bruk av en eksisterende forskningsbiobank. Dersom biobanken opprettes som en del av et spesifikt forskningsprosjekt, skal den være beskrevet i prosjektets forskningsprotokoll og inngå i ordinær prosjektsøknad til REK. Opprettelse av en generell forskningsbiobank krever en særskilt søknad til REK. Se REK portalen for mer informasjon om søknadsprosess for generell biobank. Merk at godkjenning av generelle biobanker fra REK gir kun tillatelse til innsamling og oppbevaring av materiale. Enhver bruk av dette materialet til prosjekter skal søkes til REK. REK melder alle forskningsbiobanker videre til Biobankregisteret.
- Vurder behovet for et styre: Noen biobanker krever også at det opprettes et styre i tillegg til å ha en ansvarshavende person.
- Søknad om lagring av humant biologisk materiale i Kjernefasilitet for biobank – UiT: Ta kontakt med biobank for mer informasjon.
Sist endret: 12.02.2026
Printvennlig innhold: Hvordan opprette en forskningsbiobank?
Humant biologisk materiale skal oppbevares og behandles på en forsvarlig måte med respekt for giveren – og i tråd med biobank faglig praksis. Viser til Beste praksis for norske biobanker for etablering og drift av humane biobanker. Som hovedregel skal det ikke lagres personsensitive data på prøvene og de bør derfor lagres avidentifisert/pseudonymisert.
Ansvarshavende har et selvstendig ansvar for å sikre at biologisk materiale kun brukes i tråd med avgitt samtykke og eventuelle reservasjoner. Dette innebærer at personer som har reservert seg i Registeret for biologisk forskningsreservasjon skal utelates fra utvalget før analysene gjennomføres. Se mer informasjon og hvordan dette gjøres på nettsiden til FHI og Forskeres ansvar vedrørende biologisk forskningsreservasjon.
Dersom en person er registrert i reservasjonsregisteret, kan det biologiske materialet ikke benyttes til forskning uten uttrykkelig samtykke fra vedkommende. Reservasjon mot forskning kan registreres når som helst, og må respekteres uavhengig av når materialet ble innsamlet.
Sist endret: 12.02.2026
Printvennlig innhold: Oppbevaring, behandling og bruk av biologisk materiale
Avgiver av biologisk materiale skal samtykke, enten med et spesifikt samtykke bygget på informasjon om et konkret prosjekt, eller et bredt samtykke bygget på informasjon om tematisk forskningsområde. Ved ny eller endret bruk av innsamlet humant biologisk materiale, skal det som hovedregel innhentes nytt samtykke.
Søknad om dispensasjon fra samtykke og taushetsplikt skal søkes om til REK og være godkjent før bruk av materiale kan skje.
Dispensasjon fra samtykke kan gis:
dersom det er vanskelig å innhente nytt samtykke dersom forskningen er nødvendig for å utføre en oppgave av allmenn interesse dersom samfunnets interesse i forskningen klart overstiger ulempene det kan medføre for den enkelte
Samtykke kreves ikke ved bruk av anonymisert humant biologisk materiale, men må være godkjent av REK før bruk.
Tilbaketrekking av samtykke
Et samtykke til å delta i et forskningsprosjekt kan når som helst trekkes tilbake. Ved tilbaketrekking av samtykke må forskningen på avgivers materiale opphøre, og materiale skal destrueres så fremt det ikke er bearbeidet og inngår i annet materiale. Den som har trukket sitt samtykke kan kreve at det biologiske materialet destrueres og at helseopplysninger slettes eller utleveres innen 30 dager. Dersom særlig sterke samfunns- eller forskningshensyn tilsier det, kan REK tillate fortsatt forskning på materialet og utsatt destruksjon, sletting eller utlevering til forskningsprosjektet er gjennomført.
Bruk av biologisk materiale fra helse- og omsorgstjenesten
REK kan bestemme at humant biologisk materiale som er innsamlet i helse- og omsorgstjenesten til diagnostiske og behandlingsformål, kan brukes til forskning uten innhenting av samtykke dersom:
Forskningen er av vesentlig interesse for samfunnet Hensynet til deltakernes velferd og integritet er ivaretatt Pasienten på forhånd er informert om at biologisk materiale kan brukes til forskning og har fått anledning til å reservere seg
REK kan sette vilkår for bruken av materialet.
Sist endret: 17.11.2025
Printvennlig innhold: Samtykke
Forespørsel om utlevering av materiale fra en biobank skal alltid fremsettes skriftlig til den som er ansvarshavende for biobanken. Dersom forespørselen avslås av ansvarshavende, kan vedtaket påklages til REK, som har godkjent opprettelsen av biobanken. REKs avgjørelse er endelig og kan ikke påklages videre.
Ansvarshavende skal gi andre forskere tilgang til humant biologisk materiale fra biobanker, med mindre:
- Den forskningsansvarlige selv har behov for materialet, eller
- Det foreligger særlige grunner som taler mot utlevering.
Ved vurdering av om det foreligger særlige grunner, skal det legges vekt på:
- Forskningens kvalitet og relevans
- Hensynet til giverens integritet
- Den forskningsansvarliges eget behov for materialet
Materialet kan ikke utleveres til forsikringsselskap, arbeidsgiver, påtalemyndighet eller domstol, selv om den som har avgitt materialet samtykker til dette.
Sist endret: 17.11.2025
Printvennlig innhold: Forespørsel om utlevering av biologisk materiale
Før utlevering av biologisk materiale skal ansvarshavende forsikre seg om at følgende vilkår er oppfylt:
- Mottaker har tilfredsstillende rutiner for håndtering og lagring av materialet
- REK-godkjenning foreligger
- Krav til samtykke og behandling av helseopplysninger er oppfylt. REK kan sette vilkår for både utlevering og videre bruk av biologisk materiale samt tilhørende helse- og personopplysninger. Dersom prosjektet ikke er basert på samtykke, skal kopi av REKs dispensasjon fra taushetsplikten vedlegges, sammen med en spesifikasjon av hvilke forskningsdata som ønskes utlevert
- Avgiver ikke har reservert seg mot at materiale utleveres til forskning
- Alle nødvendige avtaler skal være inngått, for eksempel samarbeidsavtale, Material Transfer Agreement (MTA) eller utleveringsavtale. Ved usikkerhet om hvilke avtaler som kreves, kan FUF HF kontaktes for veiledning
- Materialet oppbevares og sendes forsvarlig. Fremgangsmåten for forsendelse skal avklares mellom partene (F.eks. via FileSender og med krav om lagring med to faktor-autentisering)
Sist endret: 19.05.2026
Printvennlig innhold: Utlevering av biologisk materiale i biobanker
Ved opphør, nedleggelse eller overtakelse av en biobank skal ansvarshavende for biobank søke godkjenning fra REK. REK må også godkjenne prosedyren ved eventuell destruksjon av materialet.
Forskningsbiobanker som benytter kjernefasilitet for biobank ved Helsefak skal varsle kjernefasiliteten ved opphør, nedleggelse eller overtakelse av biobanken. Varslingsplikten gjelder også ved endring av ansvarshavende person.
Sist endret: 12.02.2026
Printvennlig innhold: Opphør, nedleggelse eller overtakelse av forskningsbiobank
Alle trinn i prosessen knyttet til innsamling, oppbevaring, bruk og destruksjon av biologisk materiale skal dokumenteres. Dokumentasjonen skal være tilgjengelig for kontroll fra tilsynsmyndigheter og oppbevares i henhold til UiTs retningslinjer.
Sist endret: 17.11.2025
Printvennlig innhold: Dokumentasjon og arkivering
Rutine for studentoppgaver
Når du skal skrive en studentoppgave ved Det helsevitenskapelige fakultet, er det viktig å avklare hvilke krav som stilles til prosjektet ditt. Start med å stille deg disse spørsmålene:
- Skal jeg gjennomføre medisinsk og helsefaglig forskning?
- Skal jeg behandle personopplysninger?
Før du svarer på disse spørsmålene, bør du sette deg inn i hva personopplysninger og helseforskning er.
Om du svarer ja på ett av disse spørsmålene, gjelder særlige krav for oppgaven din:
- Medisinsk og helsefaglig forskning reguleres av helseforskningsloven
- Behandling av personopplysninger reguleres av personopplysningsloven og personvernforordningen (GDPR)
Diskuter alltid med veiledere din hvilke krav som stilles for oppgaven din før du går i gang med prosjektet. Veilederen din har det overordnede ansvaret for forskningen i oppgaven din. Vi ber dere sette dere inn i retningslinjer for behandling av personopplysninger i forsknings- og studentprosjekter ved UiT.
Denne rutinen skal gi deg innblikk i de viktigste punktene du som student må kjenne til når du planlegger og gjennomfører et prosjekt.
Før du starter prosjektet, må du - i samråd med veilederen din – avklare om oppgaven krever innmelding eller godkjenning hos andre instanser. De vanligste instansene er Sikt og Regionale komiteer for medisinsk og helsefaglig forskning (REK).
Dersom du bare bruker anonyme opplysninger, trenger du ikke REK-godkjenning, innmelding til Sikt eller gjennomføre en risikovurdering av informasjonssikkerhet og personvern. For at data skal regnes som anonyme må data være anonymisert før du mottar dem. Det er ikke tilstrekkelig å pseudonymere eller anonymisere selv, for eksempel ved at du erstatter personopplysningene med nummer, kode, fiktive navn og lignende. For at prosjektet skal være fullstendig anonymt, kan heller ikke du eller veileder kjenne til forskningsdeltakernes identitet.
Behandlingstiden hos både Sikt og REK kan være lang. Meldinger og søknader må derfor sendes i god tid. Du kan ikke starte datainnsamling før alle nødvendige godkjenninger foreligger.
Sikt – personverntjenester for forskning
Dersom du skal samle inn eller behandle personopplysninger i oppgaven (f.eks. bachelor-, master-, femteårs-/hovedoppgave), må du melde prosjektet inn til Sikt via digitalt meldeskjema.
Er du usikker på om prosjektet ditt innebærer behandling av personopplysninger, kan du fylle ut første side i meldeskjemaet "Hvilke personopplysninger skal du behandle?". Dette gir deg en avklaring. Sikt kan også kontaktes for generelle råd og veiledning.
Dersom du bruker data (personopplysninger) fra et forskningsprosjekt som er forankret ved for eksempel Universitetssykehuset Nord-Norge (UNN) eller en annen institusjon enn UiT Norges arktiske universitet, skal du likevel melde inn ditt eget studentprosjekt til Sikt. Selv om dataene allerede er samlet inn i et annet prosjekt, regnes studentprosjektet ditt som et selvstendig prosjekt med egen meldeplikt.
Behandlingsansvarlig institusjon for studentprosjektet ditt er UiT. Prosjektansvarlig er veilederen din. Du kan fylle ut meldeskjemaet selv, men veileder skal gjennomgå og godkjenne meldingen før den sendes inn. Du må selv gi veilederen din tilgang til prosjektet og meldeskjemaet i Sikt-portalen.
Prosjektet skal meldes senest 30 dager før planlagt oppstart av datainnsamling. Dersom det gjøres endringer underveis, for eksempel i metode, utvalg, hvilke opplysninger som behandles eller hvordan data lagres, skal dette også meldes til Sikt.
Det er viktig at du, sammen med veilederen din, melder fra til Sikt dersom det oppstår forsinkelser eller endringer i studentprosjektet.
Regionale etiske komiteer (REK)
Det må søkes godkjenning fra REK om opplysningene du samler inn også omhandler et av følgende punkter:
- Medisinsk og helsefaglig forskning – der formålet er å skaffe ny kunnskap om helse og sykdom.
- Humant biologisk materiale – alle typer fysiske materiale fra en menneskekropp
- Helseopplysninger – informasjon om en persons helsetilstand, både fysisk og psykisk.
Søknad om godkjenning av studentprosjekter til REK skal sendes av veilederen din. I søknaden er det veileder som registreres som prosjektleder. Du som student kan ikke stå som prosjektleder eller selv søke REK om godkjenning. Dersom dere er usikre på om prosjektet krever etisk godkjenning, anbefales det å sende en fremleggingsvurdering til REK. Dere finner mer informasjon om dette i REK-portalen.
Det er viktig at du, sammen med veilederen din, melder fra til både REK dersom det oppstår forsinkelser eller endringer i studentprosjektet.
Datahåndteringsplan
UiT krever at alle prosjekter utarbeider en datahåndteringsplan (DHP). DHP er et dokument som beskriver hvordan forskningsdata gjennom hele prosjektets livsløp – fra innsamling og lagring til deling, arkivering eller sletting. Planen er et arbeidsverktøy som hjelper deg å sikre god datakvalitet, etterleve regelverk og legge til rette for framtidig gjenbruk. DHP skal utarbeides før du går i gang med prosjektet, og du bør vurdere om det er behov for oppdatering og bruke den aktivt fram til prosjektet avsluttes.
👉 Les mer om datahåndteringsplan - her finner du maler, eksempler og veiledning
Sist endret: 12.03.2026
Printvennlig innhold: Personvern, forskningsetikk og datahåndteringsplan
Risikovurdering av informasjonssikkerhet og personvern
Behandler du helse- eller personopplysninger i oppgaven din, skal det gjennomføres en risikovurdering før oppstart av prosjektet. I vurderingen skal mulige uønskede hendelser, sannsynligheten for at de oppstår, og konsekvensene dersom de inntreffer, identifiseres og vurderes. Risikovurderingen skal fylles ut av deg i samarbeid med veilederen din, ved bruk av fastsatt mal.
Veilederen din er risikoeier og skal godkjenne risikovurdering. Veilederen din har også ansvar for at den blir mottatt av kontaktperson for risikovurderinger på utdanningen din.
Klassifisering av verdier i prosjektet
Forskningsdata skal være tilgjengelig for de som trenger det (tilgjengelighet), de skal sikres mot utilsiktet og urettmessig endring (integritet), og de skal ikke være tilgjengelig for uvedkommende (konfidensialitet). Du må klassifisere verdiene i forskningsprosjektet ditt, f.eks. forskningsdata, biologiske prøver etc. Klassifiseringen danner premissene for valg av tekniske og organisatoriske sikkerhetstiltak, herunder hvilken programvare som kan benyttes, hvor data kan lagres, og hvordan de kan analyseres på en sikker måte. Ved UiT skal informasjonen klassifiseres i henhold til fire konfidensialitetsnivåer.
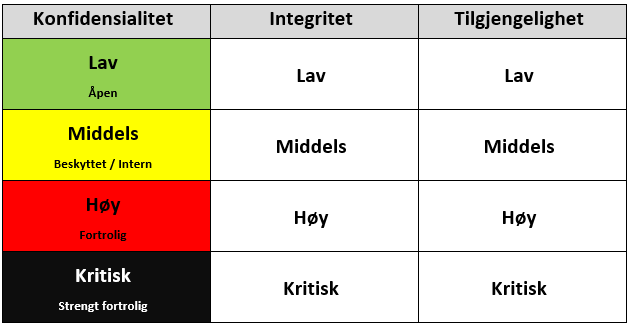
Konfidensialitetsnivåene, slikt vist til i tabellen ovenfor, er fargekodet for å tydeliggjøre graden av kritikalitet og tilhørende krav til sikringstiltak.
- Grønt nivå angir lavest kritikalitet og medfører færrest sikkerhetskrav.
- Gult nivå innebærer økt risiko og utløser strengere krav til beskyttelse.
- Rødt nivå omfatter informasjon med høy kritikalitet og stiller omfattende krav til sikring. Brudd på dette nivået kan få alvorlige konsekvenser for UiT, samarbeidspartnere og/eller enkeltpersoner.
- Svart nivå benyttes kun i særskilte tilfeller der et sikkerhetsbrudd kan medføre svært alvorlige konsekvenser, enten for UiT eller for samfunnet som helhet. Dersom informasjon vurderes klassifisert som strengt fortrolig (svart nivå), skal Faggruppe for informasjonssikkerhet og personvern konsulteres før klassifisering fastsettes.
Veilederen din er ansvarlig for å sikre at:
- informasjonen er plassert i riktig klasse
- informasjonen er vedlikeholdt, oppdatert og korrekt merket
- vurdere om forutsetningene endrer seg og man må bytte klasse sikre at informasjonen behandles i systemer og tjenester som er godkjent for dette
Lurer du på hvilke IT-systemer og tjenester du kan bruke til ulike typer data? Da må du ta utgangspunkt i klassifiseringen av data i prosjektet ditt.
Data klassifiseres som åpen (grønn), intern (gul), fortrolig (rød) eller strengt fortrolig (svart). Data skal alltid behandles – for eksempel lagres, deles og analyseres – i IT-systemer som har et sikkerhetsnivå som er tilpasset klassifiseringen.
Hvis du er i tvil om hvilken klassifisering som gjelder, bør du velge det høyeste relevante sikkerhetsnivået.
Du finner en oversikt over hvilke systemer/tjenester du kan bruke her: System og tjenester.
Sist endret: 12.03.2026
Printvennlig innhold: Risikovurdering og klassifisering
Hvis du selv skal samle inn data til studentprosjektet, må du og veileder din sørge for at deltakerne gir et frivillig og informert samtykke. Dere må utarbeide et informasjonsskriv og samtykkeskjema som gir deltakerne god informasjon om prosjektet og deres rettighet til å trekke samtykket. Bruk helst malene fra REK eller Sikt for å sikre at all nødvendig informasjon er inkludert.
Det er egne regler for innhenting av samtykke fra barn eller andre uten samtykkekompetanse:
- For barn og unge under 16 år må foreldre, eller andre med foreldreansvar, samtykke til barnets deltagelse
- Barn og unge mellom 12 og 16 år har i visse forskningsprosjekter selv rett til å samtykke til deltakelse i helseforskningsprosjekter
- Ungdom over 16 år skal samtykke på egen hånd. Ved forskning som innebærer legemsinngrep eller legemiddelutprøvinger, skal ungdom mellom 16 og 18 år samtykke sammen med foresatte.
- For personer uten samtykkekompetanse (pga. helsetilstand, psykisk utviklingshemming eller umyndiggjøring) skal nærmeste pårørende samtykke.
Det er viktig å passe på at alle samtykkeskjemaene er datert og signert på en slik måte at det er mulig å identifisere deltakeren fra signaturen. Dette kan løses ved at deltakerens navn skrives i blokkbokstaver i tillegg til signaturen.
Signerte samtykkeerklæringer i papirformat skal oppbevares forsvarlig i låst skap. Digitale samtykkeerklæringer skal oppbevares forsvarlig på et område uten tilgang for uvedkommende. De må også lagres på en slik måte at det ikke er mulig å redigere erklæringene.
Det må kunne dokumenteres at gyldig samtykke er innhentet så lenge personopplysninger behandles.
Sist endret: 17.11.2025
Printvennlig innhold: Innhenting og oppbevaring av samtykke
Forskningsdata har stor verdi og det er viktig at de lagres forsvarlig for å sikre at data ikke går tapt eller blir reduserte i kvalitet. Behandling og oppbevaring av forskningsdata kan være utfordrende, spesielt med store datasett eller data som setter spesielle krav til sikkerhet.
Hovedregelen for lagring av personopplysninger er at de oppbevares pseudonymt; det betyr at opplysningene ikke lengre kan knyttes til en forskningsdeltaker uten bruk av en koblingsnøkkel. En koblingsnøkkel er en navneliste eller fil som gjør det mulig å identifisere forskningsdeltaker i datasettet ditt. Husk at forskningsdata og koblingsnøkkel må lagres hver for seg.
Fysiske dokumenter skal oppbevares i et låst skap og i et låst rom på UiT, og kan ikke oppbevares i for eksempel studentskap på campus eller hjemme. Kun en definert brukergruppe skal ha tilgang, inkludert veilederen din. Du må avtale med veilederen din hvor disse kan oppbevares på UiT, eventuelle unntak må også avtales med veileder.
Bruk UiT godkjente programvarer/tjenester og utstyr. Dersom du bruker utstyr som ikke tilhører UiT, er det viktig at du og din veileder setter dere godt inn i, og etterlever kravene som stilles i «Rutine for bruk av privat utstyr ved behandling av personopplysninger i forsknings- og studentprosjekt».
Retningslinjer som du og veileder må gjør dere kjent med:
👉Retningslinjer for forvaltning av forskningsdata ved UiT
👉Retningslinjer for oppfølgning av datahåndteringsplaner ved UiT
Sist endret: 12.03.2026
Printvennlig innhold: Behandling og oppbevaring av forskningsdata
Behandling av helse- og personopplysninger i all forskning er av midlertidig art. Når formålet med behandlingen er oppnådd, skal forskningsdata slettes eller anonymiseres i tråd med gjeldende regelverk og prosjektets datahåndteringsplan. Dersom prosjektet har hatt godkjenning fra REK skal forskningsdata, inkludert samtykkeskjema oppbevares i fem år etter at prosjektet er avsluttet. Det er veilederen din som har ansvar for oppbevaring og sletting etter fem år.
Det er viktig at du som student ikke sitter igjen med personopplysninger etter at du er ferdig med oppgaven din – hverken i papirform eller elektronisk. Det samme gjelder for egne notater du har gjort hvor det er mulig å identifisere deltakerne.
Før prosjektet avsluttes, må du og veileder sørge for at alle nødvendige data er overført, lagret, eller slettet i henhold til datahåndteringsplanen. Diskuter med veilederen din om forskningsdataen din skal deponeres i et egnet arkiv med mål slik at andre skal kunne gjenbruke den. Et slikt arkiv kan være enten åpent eller lukket. Dere finner mer informasjon om dette i UiTs nettsider.
Dersom prosjektet har vært meldt inn til Sikt, skal du registrere prosjektet som avsluttet i Sikt-portalen.
Dersom prosjektet har hatt godkjenning fra REK er det veileder som skal sende sluttmelding via REK-portalen.
Sist endret: 12.03.2026
Printvennlig innhold: Prosjektet er ferdig - hva nå?
Avviksmeldinger er et viktig verktøy for å sikre kvalitet, etterlevelse av regelverk og trygg gjennomføring av helseforskning. Ved å melde fra om hendelser, feil, mangler eller bekymringer bidrar du til læring, forbedring og forebygging av fremtidige problemer. Bruk dette skjemaet dersom du oppdager forhold som ikke er i tråd med gjeldende rutiner, krav eller godkjenninger.
Er det behov for råd og veiledning om varsling til tilsynsmyndigheter eller spørsmål om avvik i helseforskning, kan Seksjon for forskning, utdanning og formidling ved Det helsevitenskapelige fakultet (FUF HF) kontaktes på e-post: helseforskning@helsefak.uit.no
👉 Rutine for avvik i helseforskning
👉 Avvik på HMS, informasjonssikkerhet og personvern - Si ifra!
Sist endret: 19.05.2026
Printvennlig innhold: Avvik