Avfallshåndtering: fra store byer til små celler
Når renovasjonen svikter, kan hele nabolag bli ubeboelig. Sånn er det i kroppen vår også.
Tenk deg en bydel i Tromsø, og tenk deg hvor relativt lite søppel det er i gatene. De fleste av oss kildesorterer, og vi har et velfungerende renovasjonssystem som plukker avfallet vårt opp, og deretter leverer det til nærmeste miljøstasjon. Der blir avfallet brent eller resirkulert til annet bruk.
Hva tror du skjer hvis systemet svikter og avfallet ikke blir plukket opp? Hvordan tror du nabolaget ditt hadde sett ut? Det ville selvfølgelig bli ganske fælt å bo der. Det vil lukte vondt og etter hvert vil fremkommeligheten for både fotgjengere og biltrafikk bli kraftig begrenset. Til slutt ville det blitt helsefarlig å bo der.
Det samme gjelder for cellene i kroppen vår. Hvis ikke deres renovasjonssystem fungerer vil avfall samle seg opp og forårsake uhelse og sykdom.
Selvspising
Cellene i kroppen vår kaster og resirkulerer eget avfall ved å spise det og så bryte det ned i deres tilsvarende miljøstasjon. Dette er ganske likt det som skjer når du spiser og drikker for å få energi, men bare på en mye mindre skala. Cellens avfallshåndtering blir kalt «selvspising», og cellene utfører dette for å kvitte seg med ødelagte og farlige komponenter, skaffe seg energi og holde seg sunne.
Det at cellene holder seg sunne gjennom selvspising, eller autofagi som vi forskere kaller det, er en viktig forsvarsmekanisme for å unngå at de utvikler seg til kreftceller. Kreftceller er syke celler som vokser ukontrollert og ødelegger de normale funksjonene i kroppen vår, og i verste fall kan de føre til sykdom og død.
Normale celler kan bli til kreftceller selv om avfallshåndteringen fungerer. Da kan kreftcellene gjøre et ganske sleipt grep. De kan utnytte denne selvspisingen som i utgangspunktet skulle stoppe dem, til å skaffe seg energi slik at de kan overleve og spre seg til andre deler av kroppen.
Spesialavfall
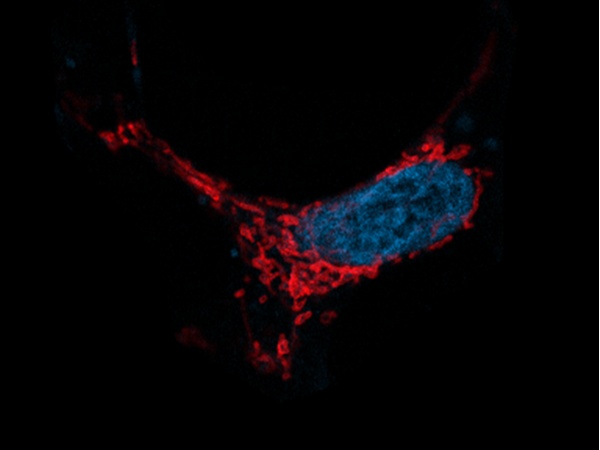
I vårt prosjekt ser vi på avfallshåndteringen til en spesifikk enhet i cellen. Disse enhetene, kalt mitokondrier, kan ses på som batteriene til cellen. Slik som alle batterier, vil de etter en tid gå tomme for energi og må kastes. Som du vet er batterier spesialavfall, som ikke kan kastes i vanlig restavfall. De må leveres til et spesielt returpunkt, og så blir de sendt videre til nærmeste miljøstasjon.
Slik er det på cellenivå i kroppene våre også. Her må batteriene i cellen spises på en spesiell måte for å kunne bli levert til miljøstasjonen. Det vi vet, er at det av og til går galt når cellenes batterier skal kastes. Vi vil finne ut mer om hvordan denne spesielle avfallshåndteringen fungerer siden, for hvis de ikke blir spist og bare hoper seg opp, kan det gjøre at normale celler blir til kreftceller. Vi har nylig publisert en engelsk fagartikkel der vi beskriver en ny brikke i denne spesielle avfallshåndteringen (Garcia-Garcia et al., 2022).
Vil gjøre kreftceller sårbare
I autofagiforskningsgruppen driver vi med basalforskning innen cellenes selvspising, autofagi. Vi ser nærmere på det helt grunnleggende i selvspising. Denne forskningen er viktig fordi den gir oss grunnlaget for å forstå hvert trinn av selvspisingen, kunnskap som er verdifull.
Ved å vite hva som er involvert i hvert trinn kan vi jobbe mer målrettet mot kreft, ettersom kreftceller kan utnytte cellenes renovasjonssystem. Hvis vi vet i hvilket trinn denne utnyttelsen skjer, og hvilke komponenter som er involvert, kan vi søke å utvikle medikamenter som forhåpentligvis kan stoppe det. Når kreftcellene ikke lenger kan bruke sine sleipe triks, kan det føre til at kreftcellene blir mer sårbare for tradisjonell behandling, og får redusert evne til å overleve og spre seg.
Les mer om autofagiforskningsgruppen ved UiT her!
Les mer om kjernefasilitet for avansert mikroskopi (KAM) her!
Referanser:
Garcia-Garcia, J., Berge, A. K. M., Overa, K. S., Larsen, K. B., Bhujabal, Z., Brech, A., Abudu, Y. P., Lamark, T., Johansen, T., & Sjottem, E. (2022). TRIM27 is an autophagy substrate facilitating mitochondria clustering and mitophagy via phosphorylated TBK1. FEBS J. https://doi.org/10.1111/febs.16628
-
Public Health - master
Varighet: 2 År -
Medisin profesjonsstudium
Varighet: 6 År -
Nordisk - årsstudium
Varighet: 1 År -
Pedagogikk - bachelor
Varighet: 3 År -
Bioingeniørfag - bachelor
Varighet: 3 År -
Informatikk, sivilingeniør - master
Varighet: 5 År -
Likestilling og kjønn - årsstudium
Varighet: 1 År -
Biomedisin - bachelor
Varighet: 3 År -
Psykologi - bachelor
Varighet: 3 År -
Ergoterapi - bachelor
Varighet: 3 År -
Fysioterapi - bachelor
Varighet: 3 År -
Radiografi - bachelor
Varighet: 3 År -
Samfunnssikkerhet - master
Varighet: 2 År -
Farmasi - bachelor
Varighet: 3 År -
Farmasi - master
Varighet: 2 År -
Psykologi - årsstudium
Varighet: 1 År -
Odontologi - master
Varighet: 5 År -
Tannpleie - bachelor
Varighet: 3 År -
Sykepleie - master
Varighet: 2 År -
Barnevern - bachelor
Varighet: 3 År -
Sosialt arbeid - bachelor
Varighet: 3 År -
Idrettsvitenskap - master
Varighet: 2 År -
Sosialt arbeid - master
Varighet: 2 År -
Vernepleie - bachelor
Varighet: 3 År -
Barnevern - bachelor
Varighet: 3 År -
Vernepleie - bachelor
Varighet: 4 År -
Ernæring - bachelor
Varighet: 3 År -
Videreutdanning i krisehåndtering og traumebehandling
Varighet: 1 År -
Videreutdanning om vold i nære relasjoner
Varighet: 1 År -
Videreutdanning i rus og psykisk helse
Varighet: 1 År -
Paramedisin - bachelor
Varighet: 3 År -
Nordisk språk og litteratur - bachelor
Varighet: 3 År -
Fysioterapi - master
Varighet: 3 År -
Aldring og geriatrisk helsearbeid - master
Varighet: 3 År -
Helsefaglig utviklingsarbeid - master
Varighet: 3 År -
Psykisk helsearbeid - master
Varighet: 3 År -
Helsesykepleie - master
Varighet: 3 År -
Jordmorfag - master
Varighet: 2 År -
Klinisk ernæring - master
Varighet: 2 År -
Velferdsendring - erfaringsbasert master
Varighet: 4 År -
Ph.d.-utdanning i helsevitenskap
Varighet: 3 År -
PhD Programme in Health Sciences
Varighet: 3 År -
Sykepleie - bachelor
Varighet: 3 År -
Psykologi profesjonsstudium
Varighet: 6 År -
Sykepleie - bachelor
Varighet: 4 År -
Samisk sykepleie - bachelor
Varighet: 4 År -
Trening, prestasjon og helse - bachelor
Varighet: 3 År -
Trening, prestasjon og helse, personlig trener - årsstudium
Varighet: 1 År -
Medisin profesjonsstudium - forskerlinje
Varighet: 7 År -
Psychology - master
Varighet: 2 År