Vi må kanskje ta antibiotika hyppigere
Vi har alle fått beskjeder om å alltid fullføre antibiotikakuren for å motvirke antibiotikaresistens. Forsking fra Centre for new antibacterial strategies (CANS) ved UiT kan tyde på at hvordan vi tar kuren også er viktig.
I løpet av en antibiotikakur varierer konsentrasjonen av antibiotika i kroppen. Like før man skal ta neste dose er konsentrasjonen på sitt laveste. Hva skjer med bakteriene og deres resistens i denne perioden?
På CANS har vi undersøkt ca. 300 generasjoner av bakterien E.coli som grodde i lave konsentrasjoner av det penicillinlignende antibiotikumet ceftazidime. Bakterien lager enzymet OXA-48 som katalyser nedbrytingen av penicillinlignende antibiotika. OXA-48 gjør at bakterier blir resistent mot mange, men ikke alle penicillinlignende antibiotika.
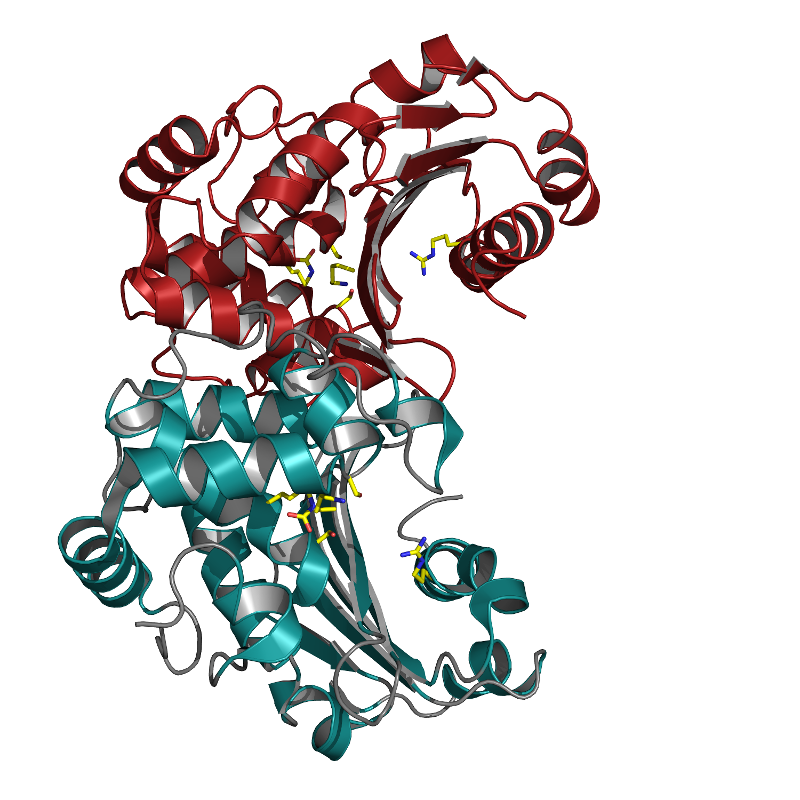
Fant 7 mutasjoner
I de 300 generasjonene fant vi 7 ulike mutasjoner i enzymet OXA-48. Vi målte resistensprofilene for mutasjonene og for noen definerte vi også den tredimensjonale proteinstrukturen, helt ned på atomnivå. Alt dette for å forstå hvordan de nye uvanlige mutasjonene, endrer egenskapene til enzymet OXA-48. Mutasjonene var på uventede plasser i den tredimensjonale strukturen, og derfor kryptiske for oss.
De 7 mutasjonene gav en svak økning i enzymaktivitet, som ikke skulle tilsi særlig mye økt resistens. Men den nye tredimensjonale strukturen og datasimuleringer med noen mutasjoner, viste små endringer i 3D-strukturen for noen av aminosyrene og mer fleksibilitet i et loopområde av enzymet. Looper er ikke rette betatråder og ikke i sirkulære helixer, så de kan lettere flytte seg uten å forbruke energi. Til sammen kan økt fleksibilitet i loopområdet forklare økningen i enzymaktivitet og at hvorfor vi kunne måle økt antibiotikaresistens.
Med andre ord, det er stor sjanse for nye uvanlige og kryptiske mutasjoner, og dermed også økt resistens når antibiotika-konsentrasjonene er lave. Slike forhold kan virke som springbrett for ytterlig nye mutasjoner som kan være langt mer kritiske for resistens enn de syv som oppstod i vårt forsøk.
Det kan også skje i kroppene våre
Så hvor finner man disse lave konsentrasjonene av antibiotika utenfor vår lab? Jo, i kroppene til dyr og mennesker, og gjerne rett før man tar en ny dose av antibiotika. Og noen plasser er det lave antibiotika-konsentrasjoner i naturen. Dette er plasser hvor mutasjonene kan vokse og velges frem.
For å unngå ytterligere økt antibiotikaresistens må man derfor se på hvordan og hvor ofte antibiotika skal doseres. Kanskje må man ta hyppigere doser? Man må og se på hva man kan gjøre for å forhindre utslipp av antibiotika til naturen. For uten fungerende antibiotika har menneskeheten et kjempestort helseproblem.
-
Fiskeri- og havbruksvitenskap - bachelor
Varighet: 3 År -
Fiskeri- og havbruksvitenskap - master
Varighet: 2 År -
Akvamedisin - master
Varighet: 5 År -
Bioteknologi - bachelor
Varighet: 3 År -
Arkeologi - master
Varighet: 2 År -
Geosciences - master
Varighet: 2 År -
Biology - master
Varighet: 2 År -
Physics - master
Varighet: 2 År -
Mathematical Sciences - master
Varighet: 2 År -
Biomedicine - master
Varighet: 2 År -
Computational chemistry - master
Varighet: 2 År -
Biologi - bachelor
Varighet: 3 År -
Medisin profesjonsstudium
Varighet: 6 År -
Luftfartsfag - bachelor
Varighet: 3 År -
Informatikk, datamaskinsystemer - bachelor
Varighet: 3 År -
Informatikk, sivilingeniør - master
Varighet: 5 År -
Geovitenskap- bachelor
Varighet: 3 År -
Biomedisin - bachelor
Varighet: 3 År -
Matematikk - årsstudium
Varighet: 1 År -
Ergoterapi - bachelor
Varighet: 3 År -
Fysioterapi - bachelor
Varighet: 3 År -
Radiografi - bachelor
Varighet: 3 År -
Farmasi - bachelor
Varighet: 3 År -
Farmasi - master
Varighet: 2 År -
Romfysikk, sivilingeniør - master
Varighet: 5 År -
Bærekraftig teknologi, ingeniør - bachelor
Varighet: 3 År -
Odontologi - master
Varighet: 5 År -
Anvendt fysikk og matematikk, sivilingeniør - master
Varighet: 5 År -
Praktisk-pedagogisk utdanning for trinn 8-13 - årsstudium
Varighet: 2 År -
Internasjonal beredskap - bachelor
Varighet: 3 År -
Ernæring - bachelor
Varighet: 3 År -
Ph.d.-program i naturvitenskap
Varighet: 3 År -
PhD Programme in Natural Science
Varighet: 3 År -
PhD Programme in Science
Varighet: 3 År -
Lektor i realfag trinn 8-13 - master
Varighet: 5 År -
Kunstig intelligens, sivilingeniør - master
Varighet: 5 År -
Fysikk og matematikk - bachelor
Varighet: 3 År -
Nautikk - bachelor
Varighet: 3 År -
Medisin profesjonsstudium - forskerlinje
Varighet: 7 År -
Havteknologi, ingeniør - bachelor (ordinær, y-vei)
Varighet: 3 År -
Informatikk, datafag - bachelor
Varighet: 3 År -
Computer Science - master
Varighet: 4 År -
Fornybar energi, sivilingeniør - master
Varighet: 5 År -
Bærekraftig kjemi og innovasjon, sivilingeniør - master
Varighet: 5 År -
Marine Biotechnology and Biological Chemistry - master
Varighet: 2 År -
Public Health - master
Varighet: 2 År -
Nordisk - årsstudium
Varighet: 1 År -
Pedagogikk - bachelor
Varighet: 3 År -
Bioingeniørfag - bachelor
Varighet: 3 År -
Likestilling og kjønn - årsstudium
Varighet: 1 År