Cellenes eget renovasjonssystem gir sunn aldring
Visste du at cellene våre har et eget renovasjonssystem? Det sørger for at kroppen vår fungerer på best mulig måte og at det ikke dannes hauger av avfall som kan føre til sykdom.

Cellenes renovasjonssystem kalles autofagi. Det er en veldig viktig prosess i cellene våre, der vi bryter ned skadede komponenter som vi ikke trenger lengre.
Autofagien baserer seg på en selektiv prosess, en slags sortering.
– Det er som om du tar støvsugeren og får bort all skitten med jevne mellomrom, forklarer professor i medisinsk biologi, Terje Johansen, som har forsket på dette i årevis.
 (1).jpg)
Han mener vi trenger forstå mer om autofagi i forhold til sunn aldring og sykdommer som akselerer aldring.
– Vi har en stadig eldre befolkning, derfor vil det bety mye for samfunnet at vi klarer å holde befolkningen sunn lengst mulig, sier Johansen.
Av den grunnen trengs det mer penger til denne typen grunnforskning.
Nobelpris til autofagi
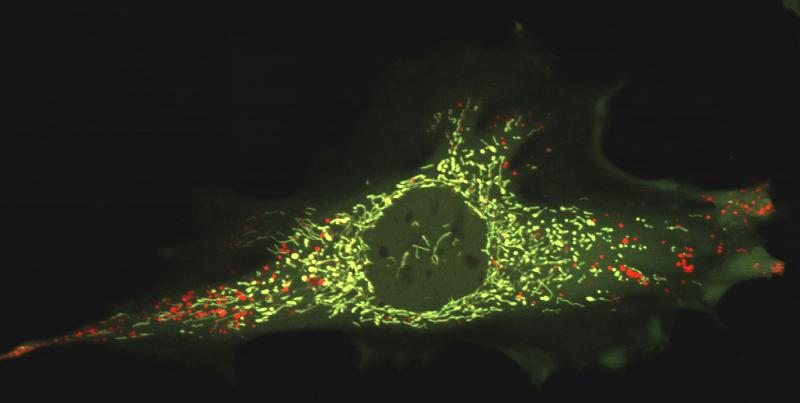
Mitokondriene – cellenes energikraftverk – trenger at autofagien er aktiv for å holde cellene våre friske. Mitokondrier som er skadde eller utslitte kan forurense og skade miljøet i cella, akkurat som en gammel dieselbil skader miljøet vårt.
Disse forurensende mitokondriene blir rensket ut av autofagien. Det er en selektiv prosess der de skadde eller dårlige mitokondriene blir fjernet.
– For å holde cella frisk, må vi få bort det som er skadelig.
Johansen og kolleger publiserte nylig en artikkel i Nature Aging der forskerne gav en oversikt over all tidligere forskning på sammenhenger mellom aldring og autofagi.
– Nobelprisen i 2016 gikk til den japanske grunnforskeren Yoshinori Ohsumi som oppdaget hvordan autofagien fungerte. Han studerte dette i bakegjær, men akkurat det samme skjer hos mennesker. Jeg var selv til stede på prisutdelingen, forteller Johansen.
Forskningsgruppa som Johansen leder, forsker på selektiv autofagi og hvordan proteinklumper i cellene våre kan bli brutt ned ved denne prosessen.
Autofagiprosessen ble tidligere sett på som en slags uspesifikk prosess for nedbrytning av materiale i cellenes cytoplasma. Forskningen til Johansen og kollegene hans har bidratt sterkt til å dreie autofagiforskninga mot selektive former for autofagi.
– Det fins aktører som oppdager de skadede komponentene. Så sender de på en måte inn noen inn for å hente søpla, putter den i søppelbilen, og kjører den av gårde til søppelplassen, forklarer Johansen.
Et eksempel på hva som skjer når et søppelsystem ikke fungerer, er da mafiaen i Napoli stoppet søppelsystemet. Det fløt over og ble kaos i byen.
– Så vi er virkelig avhengige også i kroppen vår, av at renovasjonen, dvs. autofagien fungerer, mener Johansen.
Hvorfor er autofagi så viktig?
– Det er viktig fordi det fins noen arvelige komponenter i sykdommer som gjør at proteiner klumper seg sammen og skader cellene våre. Hvis autofagien funker godt, så fjerner den klumpene, sier Johansen. For at cellene våre skal holdes friske også når vi blir eldre er det viktig at autofagien er i sving hele tida og fungerer bra.
Men hos de som har gener for arvelige sykdommer som gjør at det er en sterkere tendens til at visse proteiner klumper seg sammen i nervecellene våre kan det bli for mange klumper slik at autofagien klarer ikke å ta unna. Dette er særlig et problem når vi blir eldre og gjelder for eksempel med sykdommer som Parkinson, Huntington’s , ALS og Alzheimer.
– Alzheimer er den sykdommen som er vanskeligst for autofagien å håndtere, sier forskeren.
Hvis vi kan få autofagien til å fungere bedre hos pasienter med slike sykdommer, altså øke autofagien, så kan det hjelpe mot slike sykdommer. Det er gjort forsøk som viser dette hos for eksempel bananflue og mus.
– Det viser seg at musene kan få 17% lengre liv dersom de får et stoff som øker autofagien. Dette utgjør ganske mange år hvis vi hadde fått dette til hos mennesker, mener Johansen.
Kreften lurer naboceller
Kreft kan bruke autofagien til å stimulere sin egen vekst.
Johansen forklarer:
– Kreftsvulsten kan overtale naboceller til å gjøre ekstra autofagi for å frigjøre næringsstoffer som kreftcellen selv kan ta opp. Den kan også slå ut autofagien i sine egne celler (kreftcellene), fordi den vil ha masse mutasjoner og evolusjon for å få kreftcellene til å vokse mer.
Normale celler, på den andre siden, vil motvirke kreft og holder autofagien i gang.
– Det kreves mye grunnforskning for å forstå dette bedre. Derfor trenger grunnforskningen mer penger, understreker Johansen.
Autofagi som behandling
Kan autofagi brukes som behandling?
– Ja, det er tanken bak forskningen at det kan det i fremtiden. At vi kan manipulere nivået av autofagi, det er dit vi må komme.
Det er noen kliniske utprøvninger av kreft som pågår nå – kombinasjonsterapi. For eksempel er pankreaskreft en kreftform som er svært dødelig. Derfor gjør man nå forsøk på å hemme veksten av kreften, samtidig som man slår av autofagien. Da tror man at det er en bedre mulighet for å gjøre pasientene friske. Men behandlingene må gjøres samtidig.
– Når det gjelder Alzheimer og Parkinson forsøker man å øke autofagien, for å få den til å fjerne flere klumper, sier Johansen.
Han mener at det kommer tilbake til at vi trenger kunnskap om hva som går galt i kroppen, vi trenger grunnforskningen for å forstå hvordan det kan brukes i klinikken.
Det er en alvorlig utvikling at det bare gis penger til klinisk forskning.
– Vi må få tilbake balansen i dette. Vi bruker mye tid på å skrive søknader opp og ned, i stedet for å forske. På sikt vil det bli problemer med å rekruttere forskere til grunnforskning, tror han.
-
Fiskeri- og havbruksvitenskap - bachelor
Varighet: 3 År -
Fiskeri- og havbruksvitenskap - master
Varighet: 2 År -
Visual and Multimodal Anthropology - Master
Varighet: 2 År -
Arkeologi - master
Varighet: 2 År -
Peace and Conflict Transformation - master
Varighet: 2 År -
Indigenous Studies - master
Varighet: 2 År -
Technology and Safety - master
Varighet: 2 År -
Public Health - master
Varighet: 2 År -
Medisin profesjonsstudium
Varighet: 6 År -
Sosiologi - master
Varighet: 2 År -
Nordisk - årsstudium
Varighet: 1 År -
Strategisk ledelse og økonomi - erfaringsbasert master
Varighet: 5 Semestre -
Engelsk - årsstudium
Varighet: 1 År -
Samfunnsplanlegging - bachelor
Varighet: 3 År -
Pedagogikk - bachelor
Varighet: 3 År -
Sosiologi - bachelor
Varighet: 3 År -
Arkeologi - bachelor
Varighet: 3 År -
Bioingeniørfag - bachelor
Varighet: 3 År -
Spansk - årsstudium
Varighet: 1 År -
Statsvitenskap - bachelor
Varighet: 3 År -
Pedagogikk - master
Varighet: 2 År -
Informatikk, sivilingeniør - master
Varighet: 5 År -
Likestilling og kjønn - årsstudium
Varighet: 1 År -
Biomedisin - bachelor
Varighet: 3 År -
Samfunnsplanlegging - master
Varighet: 2 År -
Økonomi og administrasjon - bachelor
Varighet: 3 År -
Psykologi - bachelor
Varighet: 3 År -
Samfunnssikkerhet - bachelor
Varighet: 3 År -
Økonomi og administrasjon, siviløkonom - master
Varighet: 2 År -
Ledelse, innovasjon og marked - bachelor
Varighet: 3 År -
Ergoterapi - bachelor
Varighet: 3 År -
Fysioterapi - bachelor
Varighet: 3 År -
Radiografi - bachelor
Varighet: 3 År -
Grunnskolelærerutdanning for 1.-7. trinn - master
Varighet: 5 År -
Grunnskolelærerutdanning for 5.-10. trinn - master
Varighet: 5 År -
Samfunnssikkerhet - master
Varighet: 2 År -
Kunst - bachelor
Varighet: 3 År -
Kunsthistorie - master
Varighet: 2 År -
Musikkutøving - bachelor
Varighet: 4 År -
Farmasi - bachelor
Varighet: 3 År -
Farmasi - master
Varighet: 2 År -
Religionsvitenskap - årsstudium
Varighet: 1 År -
Russisk - årsstudium
Varighet: 1 År -
Samfunnsøkonomi med datavitenskap - bachelor
Varighet: 3 År -
Sosialantropologi - bachelor
Varighet: 3 År -
Organisasjonsdesign og ledelse - master
Varighet: 2 År -
Psykologi - årsstudium
Varighet: 1 År -
Statsvitenskap - master
Varighet: 2 År -
Historie - master
Varighet: 2 År -
Kunsthistorie - bachelor
Varighet: 3 År