Superbakterien som truer sykehusene
Se for deg en bakterie som kan utvikle forsvarsvåpen mot medisinene våre og som også kan dele disse våpnene med andre bakteriearter. Møt superbakterien Klebsiella pneumoniae.
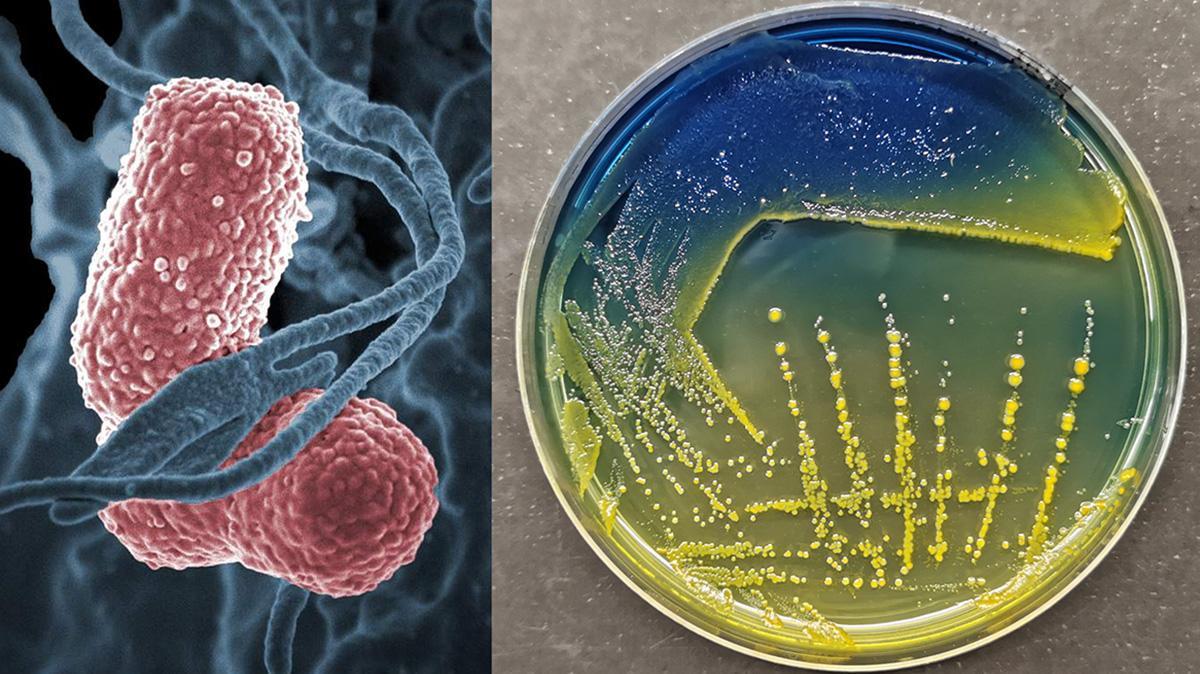

Siden penicillin ble oppdaget for nesten 100 år siden har antibiotika reddet utallige liv fra tidligere dødelige bakterieinfeksjoner. Samtidig har bakteriene utviklet en rekke ulike mekanismer for å motstå effektene av antibiotika, noe som har gjort at dagens behandling stadig blir mindre effektiv.
Disse såkalte antibiotikaresistente bakteriene utgjør en stor trussel mot helsevesenet, spesielt i sykehusmiljøer der sårbare pasienter har høy risiko for å få infeksjoner.
Globalt døde over 1,1 millioner mennesker av slike infeksjoner i 2021. I Norge er situasjonen heldigvis ikke like alvorlig, men resistensen øker også her. Men hvordan havner egentlig disse farlige bakteriene på sykehuset?
Trives overalt
I bakterienes mikroskopiske verden er Klebsiella pneumoniae en av verstingene. Mens de fleste bakterier foretrekker spesifikke miljøer, trives denne nesten overalt – i jord, på planter, i vann, og ikke minst i tarmen til både dyr og mennesker.
Ofte lever den der uten å forårsake problemer. Men kommer den på avveie til andre organer kan den raskt gi farlige infeksjoner – spesielt om den er resistent mot flere typer antibiotika, såkalt multiresistent.
På sykehus kan Klebsiella pneumoniae forårsake alt fra urinveisinfeksjon og lungebetennelse til alvorlig blodforgiftning. Når disse infeksjonene er multiresistente, blir de svært utfordrende å behandle. Dette er grunnen til at Klebsiella pneumoniae har fått status som en av de mest fryktede superbakteriene.
Hva er det som gjør denne bakterien så tilpasningsdyktig? Klebsiella pneumoniae har et stort genom (arvestoff) som gir den en imponerende verktøykasse til å overleve i forskjellige miljøer. Denne verktøykassen inkluderer også gener som gir resistens mot antibiotika, og bakterien er spesielt flink til å "låne" gener fra andre bakterier den møter – for eksempel i miljøet.
Deler antibiotikaresistens med andre bakteriearter
Det som gjør denne bakterien ekstra farlig, er at den ikke bare kan plukke opp resistensgener fra andre bakterier i miljøet, men den kan også dele de videre. Når den kommer inn på sykehuset, kan den overføre resistensgener til andre farlige bakterier, som for eksempel E. coli, og skape en kjedereaksjon hvor resistens sprer seg mellom flere bakterier.
Se for deg dette: Klebsiella pneumoniae finnes ofte i tarmen hos griser. Overforbruk av antibiotika i svineoppdrett i noen land fører til at Klebsiella pneumoniae tar opp resistens fra andre bakterier i grisens tarm.
Når personer kommer i kontakt med griser, enten gjennom direkte kontakt eller via mat, så kan antibiotikaresistente Klebsiella pneumoniae spre seg til tarmen hos menneskene.
Senere, hvis en av disse personene blir innlagt på sykehuset, kan bakterien bringes med inn i sykehusmiljøet, hvor den får muligheten til å spre resistens til andre pasienter og dele resistens med andre bakterier.
Slik kan antibiotikaresistens som utvikles hos dyr eller i miljøet finne veien til sykehuspasienter.
Akkurat dette scenarioet skjedde med et gen som heter mcr-1, som gjør bakterier resistente mot noen av våre viktigste antibiotika. Dette genet ble først oppdaget i bakterier hos griser, hvor det "hoppet over" til Klebsiella pneumoniae. Derfra har det spredt seg til mange andre bakterier og har forårsaket alvorlige problemer på sykehus verden over.
For å bremse denne trusselen jobber forskere med å utvikle nye strategier for å oppdage, forebygge og behandle infeksjoner. Analyser av arvestoff gjør det mulig å spore hvordan resistensgener sprer seg, og strenge smitteverntiltak på sykehus er avgjørende for å hindre videre spredning.
I Norge jobber det norske Klebsiella pneumoniae nettverket NOR-KLEB-NET med bakterier fra mennesker, dyr og havet for å forstå spredningen av denne superbakterien, utvikle nye metoder for overvåkning, samt undersøke alternative behandlinger mot tarmkolonisering og infeksjon.
Nettverket ledes av forskere ved UiT Norges arktiske universitet/Universitetssykehuset Nord-Norge HF og Helse Stavanger HF, og involverer partnere fra blant annet Veterinærinstituttet og Havforskningsinstituttet.
Riktig bruk av antibiotika og god håndhygiene kan redusere problemet
Men det er ikke bare opp til forskerne – alle kan bidra i kampen mot antibiotikaresistens. Å kun bruke antibiotika når det er nødvendig for pasienter både i og utenfor sykehus og begrense bruken av antibiotika i hav- og landbruket — noe vi allerede er ganske flinke på her i Norge — er noen av de viktigste måtene vi kan bremse spredningen av antibiotikaresistens på.
I tillegg kan god håndhygiene, spesielt når man besøker sykehus eller er i nærheten av sårbare mennesker, som svært gamle og unge, bidra til å forhindre spredning av farlige bakterier som Klebsiella pneumoniae.
På den måten kan du med enkle grep være med på å kjempe mot denne superbakterien.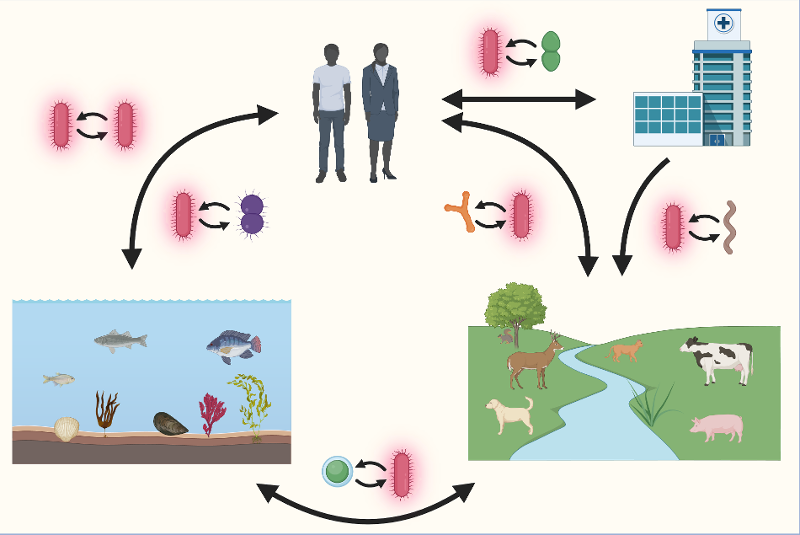 Bakterien Klebsiella pneumoniae (rød farge) kan spres fra mennesker til miljøet, og vice versa. Den trives godt i forskjellige miljøer, hvor den kan låne antibiotikaresistens fra andre bakterier og spre den videre fra et miljø til et annet. Bakterien trives i mennesketarmen og kan på sykehus gi alvorlige infeksjoner som er svært vanskelige å behandle. Laget av Kenneth Lindstedt og Marit Hetland med illustrasjonsprogrammet BioRender. Illustrasjon: Kenneth Lindstedt / Marit Hetland
Bakterien Klebsiella pneumoniae (rød farge) kan spres fra mennesker til miljøet, og vice versa. Den trives godt i forskjellige miljøer, hvor den kan låne antibiotikaresistens fra andre bakterier og spre den videre fra et miljø til et annet. Bakterien trives i mennesketarmen og kan på sykehus gi alvorlige infeksjoner som er svært vanskelige å behandle. Laget av Kenneth Lindstedt og Marit Hetland med illustrasjonsprogrammet BioRender. Illustrasjon: Kenneth Lindstedt / Marit Hetland
Vitenskapelige referanser:
(1) https://www.thelancet.com/journals/lancet/article/PIIS0140-6736(24)01867-1/fulltext
(2) https://www.fhi.no/contentassets/4e24fb63a3754577a94c42b6c8cc89c4/norm-norm-vet-2023-komplett.pdf
(3) https://www.sciencedirect.com/science/article/pii/S1369527418300225
(4) https://www.thelancet.com/journals/laninf/article/PIIS1473-3099(15)00424-7

-
Public Health - master
Varighet: 2 År -
Medisin profesjonsstudium
Varighet: 6 År -
Nordisk - årsstudium
Varighet: 1 År -
Bioingeniørfag - bachelor
Varighet: 3 År -
Informatikk, sivilingeniør - master
Varighet: 5 År -
Likestilling og kjønn - årsstudium
Varighet: 1 År -
Biomedisin - bachelor
Varighet: 3 År -
Kjemi - bachelor
Varighet: 3 År -
Psykologi - bachelor
Varighet: 3 År -
Ergoterapi - bachelor
Varighet: 3 År -
Fysioterapi - bachelor
Varighet: 3 År -
Radiografi - bachelor
Varighet: 3 År -
Samfunnssikkerhet - master
Varighet: 2 År -
Farmasi - bachelor
Varighet: 3 År -
Farmasi - master
Varighet: 2 År -
Psykologi - årsstudium
Varighet: 1 År -
Odontologi - master
Varighet: 5 År -
Tannpleie - bachelor
Varighet: 3 År -
Sykepleie - master
Varighet: 2 År -
Barnevern - bachelor
Varighet: 3 År -
Sosialt arbeid - bachelor
Varighet: 3 År -
Idrettsvitenskap - master
Varighet: 2 År -
Sosialt arbeid - master
Varighet: 2 År -
Vernepleie - bachelor
Varighet: 3 År -
Barnevern - bachelor
Varighet: 3 År -
Vernepleie - bachelor (deltid, samlingsbasert)
Varighet: 4 År -
Ernæring - bachelor
Varighet: 3 År -
Videreutdanning i krisehåndtering og traumebehandling
Varighet: 2 Semestre -
Videreutdanning om vold i nære relasjoner
Varighet: 2 Semestre -
Videreutdanning i rus og psykisk helse
Varighet: 2 Semestre -
Paramedisin - bachelor
Varighet: 3 År -
Nordisk språk og litteratur - bachelor
Varighet: 3 År -
Fysioterapi - master
Varighet: 3 År -
Aldring og geriatrisk helsearbeid - master (deltid, samlingsbasert)
Varighet: 3 År -
Helsefaglig utviklingsarbeid - master
Varighet: 3 År -
Psykisk helsearbeid - master
Varighet: 3 År -
Helsesykepleie - master
Varighet: 3 År -
Jordmorfag - master
Varighet: 2 År -
Klinisk ernæring - master
Varighet: 2 År -
Velferdsendring - erfaringsbasert master
Varighet: 4 År -
Ph.d.-utdanning i helsevitenskap
Varighet: 3 År -
PhD Programme in Health Sciences
Varighet: 3 År -
Sykepleie - bachelor
Varighet: 3 År -
Psykologi profesjonsstudium
Varighet: 6 År -
Sykepleie - bachelor (deltid, samlingsbasert)
Varighet: 4 År -
Samisk sykepleie (deltid) - bachelor
Varighet: 4 År -
Idrettsvitenskap - bachelor
Varighet: 3 År -
Medisin profesjonsstudium - forskerlinje
Varighet: 7 År -
Psychology - master
Varighet: 2 År -
Spesialistutdanning i oral kirurgi og oral medisin
Varighet: 10 Semestre







