Vil blokkere Aurora
Kjemiker Kazi Asraful Alam har i et doktorgradsarbeid forsket på en gruppe proteiner som har en meget sentral rolle i celledeling og i hvordan celler kommuniserer med hverandre. Noen ganger oppstår det feil i disse proteinene og da kan kan det oppstå kreft i blant annet tarm, magesekk, livmor og bryst. Det forskes intenst over hele verden på hvordan denne familien proteiner skal kunne stoppes når de blir defekte.
Stopper du èn stopper du alle
Den største utfordringen med å lage medisiner eller inhibitorer som kan blokkere dysfunksjonelle proteiner er ifølge kjemikeren at de er nesten identiske med en mengde andre proteiner som er livsviktige for overlevelse.
-Blokkering av ett kreftfremkallende protein kan i samme slengen blokkere funksjonen til en mengde andre proteiner vi trenger, utdyper han.
Alam har studert blant annet Aurora kinase, som er medlem i en stor familien av kommunikasjonsproteiner som kalles Protein kinaser. Det finnes over 500 proteiner i denne familien, og likheten er stor selv om de opptrer med ulike funksjoner i mange ulike organer.
-Likheten deres er et kjempeproblem for utvikling av gode kreftmedisiner forklarer Alam og en utfordring mange jobber med. Jeg har sett på detaljer i og rundt reaksjonssenteret for å se på hvordan vi kan designe inhibitorer som tar ut defekte proteiner men uten å blokkere funksjonen til friske proteiner.
Aurora kinase - et protein fra polområdet
Om cellen er en liten klode – opererer dette proteinet nært nord- og sørpolen. Rett før en celle skal dele seg samles arvematerialet, altså kromosomene, nært «ekvator» for kopiering. Etter kopiering bidrar Aurora kinase blant annet med å trekke hver av kopiene av arvematerialet til hver sin side, til hver sin pol kan vi si, før cellen deles på midten og resulterer i to like celler. Derav det flotte navnet relatert til himmelfenomenet som opptrer ved klodens polområder. Når Aurora kinase ikke fungerer som den skal, kan celledelingen gå ut av kontroll og forårsake kreft.
Vil stenge kommandolinjen til kreftceller (UiT nyhetsak 19. mai 2017)

Tredimensjonale datamodeller
Alam beskriver arbeidet sitt som en god blanding av eksperimentelle forsøk på laboratoriet og datasimuleringer, der oppbygningen til Aurora kinasene er studert i tredimensjonale modeller. Han har studert hvordan aminosyrer i reaksjonssenteret binder til ulike inhibitorer og hvordan de binder internt til hverandre.
-Disse kinasene er fleksible i konsistens, de er på en måte litt myke og føyelige, det er derfor utfordrende å lage gode modeller av proteinet og finne inhibitorer (medisiner) som binder perfekt til defekte kinaser.
Spennende funn
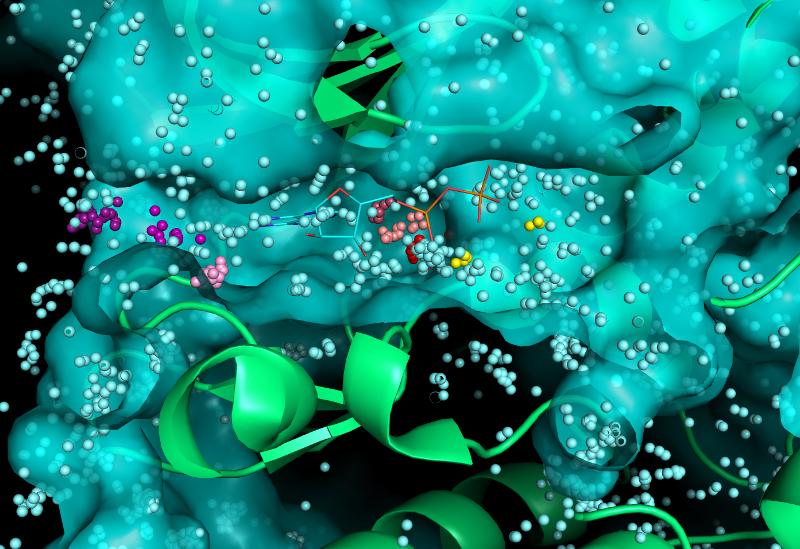
Forskeren forteller at vannmolekyler sin rolle i bindingen mellom inhibitor og protein var en spennende oppdagelse.
-I reaksjonssenteret finnes det mange vannmolekyler som tilsynelatende surrer rundt uten mål og mening, men vi fant ut at vannmolekyler har en veldig sentral rolle i hvor godt en inhibitor binder til kinasene. Molekylene skaper en bro av kontakt mellom ulike deler i det reaktive senteret og øker både selektivitet og styrke i bindingen. Dette har vi utforsket nærmere ved å bytte ut aminosyrer i reaksjonssenteret på Aurora kinase.
Alam forklarer at innsetting av hydrofobe (vannavstøtende) aminosyrer fører til at vannmolekylene presses bort, mens innplassering av hydrofile (vanntiltrekkende) grupper vil dra vannmolekylene inn i reaksjonssenteret der de kan delta i interne bindinger.
-Dette funnet gir oss noen nye ideer om hvordan inhibitorer kan designes for å bli mer spesifikke, og kan forhåpentligvis bidra til at vi kommer ett skritt nærmere en løsning på hvordan vi skal klare å lage kreftmedisiner som skiller bedre på kreftfremkallende og “friske” proteiner.
Alam var tilknyttet forskerskolen BioStruct mens han jobbet med doktorgradsarbeidet sitt og ble veiledet av Richard Engh, Institutt for kjemi, UiT-Norges arktiske universitet.
Les mer:
Doktorgradsavhandling: Studies on selectivity determinants of protein kinase inhibitor (Munin, UiT vitenarkiv)



